HBV増殖抑制に重要なIFN誘導性タンパク質とそのメカニズムは?
横浜市立大学は1月28日、B型肝炎ウイルス(HBV)感染細胞におけるウイルスの増殖抑制に、インターフェロン誘導性タンパク質であるガレクチン-9(GAL9)が関わっていることを発見したと発表した。この研究は、同大大学院医学研究科微生物学の梁明秀教授、宮川敬准教授らの研究グループが、国立感染症研究所、国立国際医療研究センター研究所などとの共同研究として行ったもの。研究成果は、「Nature Communications」に掲載されている。
画像はリリースより(詳細は▼関連リンクからご確認ください)
世界保健機関の報告によると、世界中で約20億人がHBVに感染していると推計されており、そのうち2億4,000万人以上が肝硬変や肝細胞がんに進行するリスクのある慢性B型肝炎に罹患している。現在、慢性B型肝炎に対する核酸アナログ製剤による治療法は、肝硬変や肝細胞がんへの進行を防ぐことを目的としており、HBVそのものを排除することは難しいとされている。また、核酸アナログ製剤による治療が長期におよぶと副作用のリスクが高くなるとともに、薬剤耐性ウイルスが出現し、治療の失敗と病気の進行につながる可能性がある。したがって、これらの課題を克服した新たな抗ウイルス療法が待ち望まれている。
慢性B型肝炎の治療法の一つが、インターフェロン投与(IFN療法)だ。ウイルス増殖抑制効果が強く、免疫を活性化する作用もあるため、古くから慢性B型肝炎の治療に使われてきた。しかしIFNによるウイルス抑制のメカニズムについては十分に解明されていなかった。そこで研究グループは、HBV増殖抑制に重要な役割を果たすIFN誘導性タンパク質の同定とそのメカニズムの解明に挑んだ。
肝細胞のGAL9によりオートファジーが誘導され、HBVタンパク質が分解されていた
ヒト肝細胞においてI型IFNによって特異的に発現が誘導される130のインターフェロン刺激遺伝子(Interferon Stimulatory genes:ISG、ここでは「hepato-ISG」と呼ぶ)のcDNAライブラリーを作製し、生物発光共鳴エネルギー伝達法(BRET法)を用いて、HBVのコアタンパク質(HBc)と結合する遺伝子産物をスクリーニングした。その結果、10種類のhepato-ISGタンパク質がHBcと相互作用し、そのうち、ガレクチン-9(以下、GAL9)と呼ばれるタンパク質がHBVの放出を著しく減少させることがわかった。
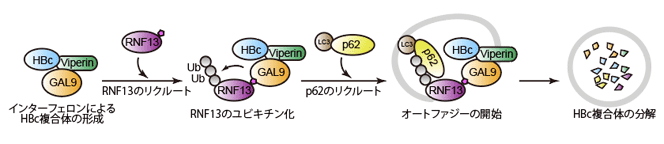
GAL9を肝細胞において発現させたところ、GAL9とHBcは細胞内に斑点状に凝集した。さらにこのような細胞では、HBVの複製が顕著に低下していた。この凝集体を調べたところ、別の抗ウイルス因子であるViperinやユビキチンリガーゼRNF13、オートファジー受容体p62などが含まれることがわかった。GAL9による抗HBV作用について詳しく解析した結果、GAL9はまずViperinを介してHBcと結合し、RNF13がリクルートされ、そのユビキチン化を促進していた。このユビキチン鎖にp62がリクルートされ、オートファジーが開始されることがわかった。
GAL9とViperinの両方がI型IFNによって誘導されることから、HBVに感染した肝細胞では、これらの因子がIFN依存性のHBc分解に相乗的に作用していることがわかった。この機構はヒトが本来もつ宿主防御機構の一部であると考えられる。ウイルス感染における自然免疫系と選択的オートファジーのクロストークが、HBVタンパク質の排除に重要な役割を果たしていることが明らかになった。
「GAL9誘導の抗ウイルス活性増強」が新たな治療戦略となる可能性
今回の研究で発見された、GAL9により誘導される抗ウイルス活性を増強する戦略により、HBVに対する新たな治療介入を可能にすることが期待される。さらに、比較的長い期間の慢性感染において、HBVがIFNによって誘導される宿主の免疫応答を回避するメカニズムを分子レベルで詳細に解明することで、既存の抗ウイルス療法と組み合わせてHBVを排除するための、より効果的な治療戦略の提案を行うことが可能になると、研究グループは考えている。
▼関連リンク
・横浜市立大学 プレスリリース




