不整脈源性心筋症の発症原因で、高頻度に同定されるPKP2変異
大阪大学は1月21日、不整脈源性心筋症の病態をヒトiPS細胞由来分化心筋細胞により解明したと発表した。この研究は、同大大学院医学系研究科の肥後修一朗特任准教授(常勤)(重症心不全内科治療学)、宮川繁教授(心臓血管外科学)、坂田泰史教授(循環器内科学)らの研究グループによるもの。研究成果は、「Stem Cell Reports」に掲載されている。
画像はリリースより
不整脈源性心筋症は、主にゲノム遺伝子異常による心筋の障害から、致死性不整脈による突然死や心不全に至る重篤な疾患群として定義される。細胞と細胞をつなぐデスモゾームを構成する遺伝子の変異は、不整脈源性心筋症の発症原因となることが知られ、中でもPKP2遺伝子変異は、最も高頻度に同定されている。不整脈源性心筋症では、不整脈とともに心筋収縮力の低下を来すが、その詳細な分子メカニズムは明らかでない。そのため、病態を再現し得る精密なヒト疾患モデルの確立が必要とされていた。
PKP2タンパク質減少に伴い心筋収縮力低下、デスモゾーム形成異常確認
研究グループは、PKP2遺伝子の2つの対立遺伝子のうち片方だけに変異があるヘテロ接合型フレームシフト変異により不整脈源性心筋症を発症した症例より、iPS細胞(PKP2変異/野生型)を樹立。ゲノム編集を用いて、ヘテロ接合型変異を正常に修復したiPS細胞(野生型/野生型)、および両方の対立遺伝子にフレームシフト変異を導入したiPS細胞(PKP2変異/PKP2変異)を作製した。これら遺伝背景が同一の細胞セットを心筋に分化させ、シート状に拍動する心筋の経時的なモーションベクトル解析により、PKP2タンパク質の減少に伴い、心筋収縮力が低下、興奮伝播が障害されることが明らかとなった。
さらに、デスモゾームタンパク質DSG2が、PKP2の完全欠損により細胞の辺縁から脱落すること、PKP2の半分量への減少により形成阻害を来すことも明らかとなった。
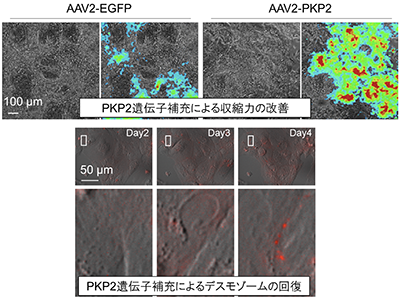
AAVでPKP2遺伝子導入、低下した収縮力改善、脱落したデスモゾーム回復
デスモゾーム動態をより詳細に解析するため、構築した3つの細胞セットにさらにゲノム編集を行い、DSG2遺伝子の片方のアレルに特異的に赤色蛍光タンパク質(tdTomato)を挿入したイメージング細胞セットを樹立。タイムラプスイメージングを行うことで、iPS細胞から心筋細胞への分化の過程におけるデスモゾームの変化、拍動する心筋細胞におけるデスモゾームの動態を生きた細胞で観察することが可能となった。
蛍光標識されたDSG2-tdTomato融合タンパク質は内在性遺伝子と同様の挙動を示し、拍動心筋でPKP2欠損によるデスモゾーム形成低下が観察された。PKP2変異iPS分化心筋細胞、デスモゾームイメージングiPS分化心筋細胞にアデノ随伴ウイルス(AAV)を用いてPKP2遺伝子を導入したところ、低下した収縮力が改善し、脱落したデスモゾームが回復する過程が経時的に観察された。
難治性心筋症への治療法開発で、有用なプラットフォーム提供に期待
不整脈源性心筋症では、既存の心不全治療薬が奏功せず進行した場合、心臓移植しか治療方法がない。研究グループは、「PKP2タンパク質が欠損したiPS分化心筋細胞を用いて、その病態解明を行い、遺伝子補充の治療概念を実証した。精密に遺伝子を改変した不整脈源性心筋症モデル細胞、およびデスモゾームを可視化するイメージング細胞は、難治性心筋症に対する今後の治療法開発において、有用なプラットフォームを提供すると考えられる」と、述べている。
▼関連リンク
・大阪大学 ResOU



