線維化進行抑制の治療効果、臨床試験等の短い観察期間での評価は困難
広島大学は12月28日、長期的な肝線維化進行を予測する肝臓の遺伝子発現パターンの同定に成功したと発表した。この研究は、同大大学院医系科学研究科消化器・代謝内科学の大野敦司助教ら、米国University of Texas Southwestern Medical Center(Dr. Yujin Hoshida研究室)および医療イノベーション共同研究講座の茶山一彰教授らの研究グループによるもの。研究成果は、「Gastroenterology」電子版に掲載されている。
画像はリリースより
世界では、年間122万人が肝硬変で死亡し、その数は過去20年間で46%増加している。さらに、肝硬変は、世界のがん死亡原因の第4位である肝がんの主要な原因とされている。線維化が進行し、肝硬変に至るには通常20~30年かかるため、線維化進行を抑制する治療の効果を臨床試験等の短い観察期間で評価することは現実的に困難だ。そのため、長期間内服を継続することにより、線維化進行を抑制できる薬であったとしても、一般的な臨床試験の期間内で効果を判定した場合には効果なしと判定される可能性もある。
研究グループは、長期的な線維化の進行を予測する信頼性の高い代替バイオマーカーがあれば、その代替マーカーの変化の評価で、抗線維化療法の効果を臨床試験の様な短い時間枠の中でも推定することが可能になると考え、同研究を計画した。
初回評価時FPS高リスク症例、線維化進行の可能性が高い
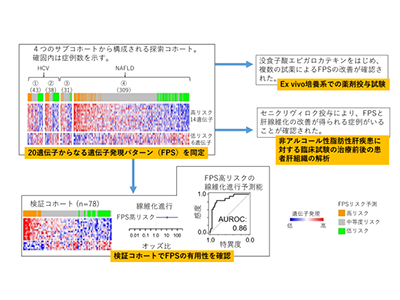
まず、C型慢性肝炎、または、非アルコール性肝疾患患者、計421人の肝組織の網羅的遺伝子発現データを用いて、長期的な肝線維化進行に関わる20個(発現が高いと線維化が進行するリスクが高い高リスク遺伝子14個、発現が高いとリスクが低い低リスク遺伝子6個で構成される)を同定。この20個の遺伝子の発現パターンをここではFibrosis Progression Signature(FPS)と呼ぶことにした。例えば、高リスク遺伝子の発現が高く、低リスク遺伝子の発現が低い場合は、FPS高リスク、その逆の場合はFPS低リスクと判定される。
次に、同定されたFPSの線維化進行予測能について、別の独立した集団(非アルコール性肝疾患患者78人)で検証。病理学的に肝線維化の評価を行った際の肝組織を用いて、FPSにより低リスク群、中等度リスク群、高リスク群に分類した。この集団では、中央値2.4年後にも再度病理学的評価を行っており、線維化ステージが1つ以上進行した場合に、線維化進行と定義。その結果、初回評価時にFPS高リスクだった症例では、線維化進行の可能性が高いということがわかった(オッズ比10.93、p=0.04)。また、ROC曲線(Receiver Operating Characteristic Curve)にて、FPSの線維化進行例と非進行例を識別する能力を評価。その結果、AUC 0.86と良好な結果だった。
没食子酸エピガロカテキンなどで、FPSを調整できる可能性
次に、慢性肝疾患患者の肝組織スライスを用いたEx-vivo培養系を用いて、13種類の抗線維化治療候補となる薬剤がFPSに与える影響について調査。その結果、没食子酸エピガロカテキンなど、いくつかの薬剤により、FPSを良い方向に調整できる可能性が示された。
さらに、臨床試験で、CCR2/5拮抗薬セニクリヴィロクを投与された非アルコール性肝疾患患者の治療前後の肝組織のFPSを調査。その結果、FPSの改善は治療開始1年後の肝線維化の改善に関連していることがわかった。
長期的な線維化進行抑制効果、臨床試験期間内での評価に期待
研究グループは、今回の研究で同定されたFPSについて、将来的に、線維化が進行する症例を高精度に予測でき、また、治療介入により、FPSを改善させることができることがわかったとしている。
このことから、臨床試験のアウトカムとしてFPSの変化を評価することにより、長期的な線維化進行の抑制効果を、一般的な臨床試験の期間内に評価できるようになると期待される、と研究グループは述べている。
▼関連リンク
・広島大学 研究成果



