タウタンパク質に対する脳内ミクログリアの反応メカニズムは?
東京医科歯科大学は11月15日、アルツハイマー病(AD)をはじめとして、前頭側頭葉変性症、パーキンソン病、ハンチントン病など複数の神経変性疾患の病態に関与するタウタンパク質が、脳内ミクログリアにおいて、エイズウイルスの細胞内受容体として知られているPQBP1に認識されて、脳炎症を誘発する分子メカニズムを発見したと発表した。この研究は、同大難治疾患研究所/脳統合機能研究センター神経病理学分野の岡澤均教授の研究グループと、富山大学、創価大学との共同研究によるもの。研究成果は、「Nature Communications」に掲載されている。
画像はリリースより
2025年には高齢者の5人1人が認知症に罹患するといわれており、その原因となるアルツハイマー病、前頭側頭葉変性症、あるいはパーキンソン病に関連するレビー小体型認知症などが大きな問題となっている。また、異常タンパク質の蓄積・凝集によって発症するハンチントン病などの神経変性疾患も認知症の原因となりえる。
これらの複数の神経変性疾患に共通して、タウというタンパク質が病態に関与することが知られている。例えば、アルツハイマー病と前頭側頭葉変性症の一部では、タウタンパク質が神経細胞の中で蓄積・凝集して神経細胞死を誘発すると同時に、タウタンパク質は神経細胞から細胞外に放出されて、脳の炎症を誘発する、あるいは脳の離れた場所の神経細胞に取り込まれるなどして悪影響を与えると考えられている。脳には、全身組織の免疫系の司令塔といわれるマクロファージに相当するミクログリアという免疫細胞が存在するが、ミクログリアがタウタンパク質に対して、どのような分子メカニズムを用いて反応しているかは、十分に解明されていなかった。
エイズウイルスの細胞内受容体としても知られる分子「PQBP1」に着目
岡澤教授の研究グループは、1998年にポリグルタミン配列に対する結合タンパク質としてPQBP1という分子を発見。ハンチントン病や脊髄小脳失調症の原因タンパク質にはグルタミンが繰り返すポリグルタミン配列が含まれることが多く、しかも、ポリグルタミン配列中のグルタミンの繰り返し数が増えると病気を発症することが知られている。また、同研究グループは、これらの神経変性疾患の病態を担う候補分子としてPQBP1を発見していた。実際、PQBP1はハンチントン病や脊髄小脳失調症の原因タンパク質と結合することで、転写やDNA損傷修復機能が低下して発症につながることも確認された。さらに、アルツハイマー病においても、別な病態経路からPQBP1の機能低下が起こり、これが神経細胞機能の低下につながることもわかっている。
PQBP1に先天的な遺伝子変異があると、患者の知的機能が低下することも、欧州の多施設共同研究から解明されていた。一方、米国Sanford-Burnham医学研究所は、免疫系細胞のマクロファージにおいて、ヒト免疫不全ウイルスHIV(エイズウイルス)をマクロファージ細胞が検知する際の細胞内受容体としてPQBP1が機能していることを発見していた。
そこで、岡澤教授の研究グループは、マクロファージに相当するミクログリアが、複数の神経変性疾患タンパク質と結合することが知られているPQBP1を介して、タウタンパク質に対して反応しているのではないかという仮説を立て、検証した。
PQBP1欠損により、ミクログリアのタウタンパク質に対する炎症反応は極端に低下
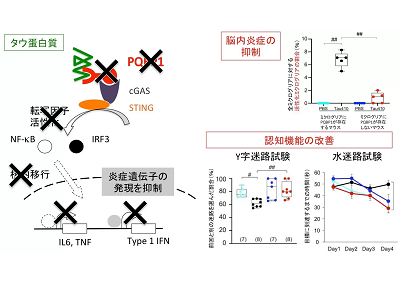
実際に実験を行ったところ、想像したように、タウタンパク質はPQBP1と結合することが物理的に証明され、ミクログリアに取り込まれた後に、細胞の中でもタウタンパク質はPQBP1と結合していたことがわかった。また、ミクログリアの中のPQBP1を欠損させると、ミクログリアのタウタンパク質に対する炎症反応は極端に低下することが、培養ミクログリアあるいは脳内ミクログリアにおいて観察された。特に、タウタンパク質を脳内に注入するとマウスは認知症の症状をきたすが、ミクログリア特異的にPQBP1を欠損させたマウスにおいては、脳炎症と同時に認知機能低下も大幅に改善されたという。
原因物質レベルでウイルス感染症と神経変性疾患の分子メカニズムの共通性を示す
今回の研究では、ウイルス感染症と神経変性疾患が、それぞれの代表的疾患病態(エイズとタウ関連疾患)において、同じ分子メカニズムを介してミクログリア炎症を引き起こしていることが明らかになった。ウイルス感染症と神経変性疾患は、ともに細胞内封入体を作ることがある、スローウイルス感染症の臨床症状が神経変性疾患と共通している、日本脳炎後にパーキンソン病様の症状になることがある、など共通性に関する断片的な知識が蓄積している。しかし、両者の詳細な関係はよくわかっておらず、今回の研究のように、原因物質レベルでウイルス感染症と神経変性疾患の分子メカニズム(ミクログリアの感知システム)が共通していることを示したのは、初めてのケースである可能性があるという。
一方、近年は、アルツハイマー病のもう一つの原因物質であるアミロイドが、病原体をトラップする自然免疫系の防御物質であるという仮説も提唱されている。抗体などの獲得免疫系が進化する前から身体に備わっていた自然免疫系と、神経変性疾患との関係についての研究が急速に進歩しており、今回の研究成果が契機となって、ウイルス感染症と神経変性疾患が互いにどのように影響を与えるのかについての理解が進むことが期待される。
また、今回の研究成果から、PQBP1のミクログリアにおける病態機能が解明された。先行研究では、アルツハイマー病態下のニューロンにおけるPQBP1の機能が明らかになっていた。「脳のそれぞれの細胞でPQBP1機能を適切に調節することが、神経変性疾患病態からの回復、さらには生理的状態での脳機能活性化につながる可能性も生まれた。これらの知見が将来的に革新的な治療法に発展することも期待できる」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




