治療抵抗性となった治癒切除不能な進行・再発のHER2陽性大腸がん対象
国立がん研究センターは11月12日、HER2陽性大腸がん患者を対象に、抗HER2抗体療法であるペルツズマブとトラスツズマブの併用療法の有効性と安全性を評価する医師主導治験(TRIUMPH試験、EPOC1602)を実施し、その結果を発表した。同試験は、同センター東病院を中心に、全国7施設で実施された。研究成果は、「Nature Medicine」オンラインに掲載されている。
画像はリリースより
HER2陽性大腸がんは、大腸がんの2~3%でしか認められず、国内外で承認された薬剤がないアンメットメディカルニーズの高い希少なサブタイプである。国立がん研究センター東病院は、HER2陽性大腸がんのように消化器がんの希少なサブタイプを同定することを目的として、2015年にSCRUM-Japanを設立し、消化器がん患者の腫瘍組織遺伝子パネル検査を行うGI-SCREEN-Japanを開始。2018年1月から、進行消化器がん患者の血液をリキッドバイオプシーとして解析するスクリーニングプロジェクト「GOZILA Study(ゴジラ・スタディ)」を米国Guardant Health(ガーダントヘルス)社との共同研究として開始している。
2018年1月から開始されたTRIUMPH試験は、治療抵抗性となった治癒切除不能な進行・再発のHER2陽性大腸がん患者を対象に、ペルツズマブとトラスツズマブの併用療法の有効性と安全性を評価する多施設共同第2相医師主導治験。国立がん研究センター東病院を中心に、全国7施設で実施された。
登録症例の約30%で奏功、有効性評価基準上回る結果
対象患者は、腫瘍組織遺伝子パネル検査またはリキッドバイオプシーでスクリーニングを行った。腫瘍組織遺伝子パネル検査には、GI-SCREEN-Japanの基盤を活用し、HER2のIHC法/FISH法を実施し、国立がん研究センター東病院が米国、韓国の研究グループと共同で策定した診断基準に基づき、HER2陽性大腸がんの判定を行った。リキッドバイオプシーを用いたスクリーニングはGOZILA Studyで行われ、米国Guardant Health社のGuardant360(R)(ガーダントスリーシックスティ)が用いられた。腫瘍組織遺伝子パネル検査147例、リキッドバイオプシー1,107例をスクリーニングし、そのうちHER2陽性大腸がんと診断された30例(腫瘍組織遺伝子パネル検査:27例、リキッドバイオプシー:25例)がTRIUMPH試験に登録され、ペルツズマブとトラスツズマブの併用療法を受けた。
その結果、腫瘍組織遺伝子パネル検査でHER2陽性の患者では30%(27例中、部分奏効以上が8例)、リキッドバイオプシーではHER2陽性の患者で28%(25例中、部分奏効以上が7例)の奏効割合が得られた。これらの結果は、あらかじめ設定した有効性評価基準(25人中5人以上の部分奏効)を上回るものだった。
またSCRUM-Japanレジストリに登録されたHER2陽性大腸がん患者のうち、同試験に参加した患者と同様の基準を満たした13例では、抗がん剤治療による腫瘍の縮小は全く見られなかった。従って、ペルツズマブとトラスツズマブの併用療法は、治療に抵抗性となったHER2陽性大腸がん患者にとって、従来使用されていた抗がん剤と比べて優れた有効性がある可能性があることがわかった。
リキッドバイオプシーによる経時的な検査で、有効性が高い可能性を示す特徴を複数発見
研究では、患者個々の遺伝子情報と有効性の関連を調べるため、腫瘍組織遺伝子パネル検査やリキッドバイオプシーによる経時的な検査も行われた。その結果、治療前の腫瘍組織遺伝子パネル検査、リキッドバイオプシーそれぞれで、「HER2の遺伝子コピー数が多い」「他のがんゲノム異常が併存していない」患者では、それ以外の患者と比べて有効性が高いことが見出された。
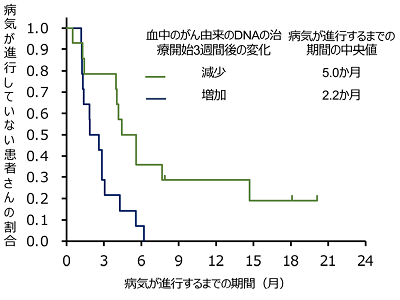
また、治療開始3週間後のリキッドバイオプシーにより、「血中循環腫瘍DNA(ctDNA)が治療開始前より減少している」患者で有効性が高いこともわかった。これにより、リキッドバイオプシーを繰り返し行うことで、有効性を予測できる可能性が示唆された。さらに、治療が効かなくなった後のリキッドバイオプシーによる結果で、さまざまながんゲノム異常が新しく出現していることが判明した。今後はこれら新しく出現したがんゲノム異常も考慮することで、HER2陽性大腸がんの治療をより改善できる可能性がある。
リキッドバイオプシーが大腸がんの治療薬選択や有効性の予測に活用される可能性
今回の研究成果により、世界初となるHER2陽性大腸がん患者に対する有効な治療法の誕生につながることが期待される。またリキッドバイオプシーが大腸がん患者に対する治療薬の選択や有効性の予測、耐性因子の発見に活用されていく可能性がある。国立がん研究センター東病院は、「製薬企業が積極的に取り組みにくい希少なサブタイプに対して有効な治療を開発するため、SCRUM-Japanの基盤を活用してスクリーニングプラットフォームの構築や医師主導治験の実施に積極的に取り組んできた。今後も一人でも多くの患者が最善の治療を受けられるよう、がん個別化治療の実現を目指す」と、述べている。
なお、研究成果を基に、中外製薬株式会社は、HER2陽性大腸がんに対するペルツズマブとトラスツズマブの併用療法を2021年4月に承認申請している。
▼関連リンク
・国立がん研究センター プレスリリース




