開発した計算モデルで、ドーパミン減少によるシナプス可塑性の謎に迫る
生理学研究所は10月1日、ドーパミンの情報伝達におけるアクセルとブレーキのバランスの崩れが学習・記憶に異常をもたらすことを、計算モデルを用いて示したと発表した。この研究は、同研究所の浦久保秀俊特任助教、窪田芳之准教授らの研究グループと、東京大学大学院医学系研究科の河西春郎教授(東京大学国際高等研究所ニューロインテリジェンス国際研究機構主任研究者)および柳下祥講師、京都大学大学院・情報学研究科の石井信教授(同・連携研究者)との共同研究グループによるもの。研究成果は、「PLoS Computational Biology」に掲載されている。
画像はリリースより
ドーパミンの情報伝達は、動物の学習・記憶に重要であるとともに、その異常は統合失調症をはじめとするさまざまな精神疾患・運動障害に関係することが知られている。また、学習や記憶にはシナプス可塑性と呼ばれるシナプスの柔軟な変化が重要であること、線条体と呼ばれる脳の領野においては、シナプス可塑性はドーパミン信号の一過的な減少(ドーパミン減少)を引き金に生じることがわかっている。
しかしドーパミンの情報伝達は非常に複雑で、さまざまな要因が関わっているため、個々の症例や実験から、総合的に精神疾患・運動障害の原因を理解することは難しいのが現状だ。そこで研究グループは、これまでドーパミンの複雑な情報伝達を説明する計算モデルの開発を進めてきた。計算モデル上のさまざまなパラメータを操作・観察することで、ドーパミン異常による病気の原因を予測することが可能になり、治療に役立つ可能性がある。これまでの研究で、シナプス可塑性を導く情報伝達の計算モデルの開発に成功していたが、「ドーパミン減少」が、どのようにシナプス可塑性を導いて学習や記憶を行っているのか、メカニズムは不明だった。
精神疾患・運動障害ではドーパミン減少の伝達に必要な分子濃度のバランスが崩れていた
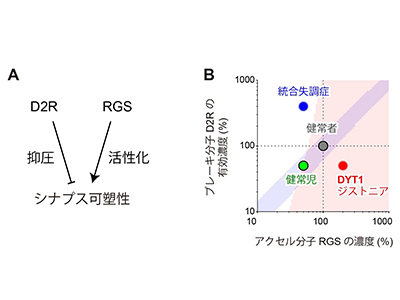
研究グループは、開発した計算モデルの詳細な解析から、ドーパミン減少が有効に伝達されるためには、アクセル分子とブレーキ分子の濃度バランスが重要であることを発見した。D2R(ドーパミンD2受容体)は、ドーパミン信号を抑制し、ブレーキをかける働きをもつ。一方で、RGS(regulator of G protein signaling)はドーパミンの信号を活性化し、アクセルをかける働きをする。複雑な計算モデルからドーパミン減少が伝達される条件を抽出・定式化したところ、「アクセル分子RGSとブレーキ分子D2Rの濃度のバランスがとれている」「アクセル分子RGSの濃度が十分に高い」という2つの条件が必要であることが明らかになった。
実際に、生体内でのアクセル分子とブレーキ分子の濃度を測った過去の実験と照らし合わせたところ、正常なマウスでは両分子の濃度は成長に伴ってともに上昇し、バランスが保たれることを再発見した。統合失調症では、ブレーキ分子は過剰に活性化するがアクセル分子は減少しており、ブレーキ分子側へバランスを崩している。反対に、運動障害の一種であるDYT1ジストニアでは、ブレーキ分子が減少する一方、アクセル分子濃度は増大し、アクセル分子側へとバランスを崩している。実際に、統合失調症ではシナプス可塑性が生じにくくなること、DYT1ジストニアではシナプス可塑性が過剰に生じることも報告されている。今回、いずれの実験結果も計算モデルの予測と合致した。
これらの結果から、健康な脳においてはドーパミン減少の伝達に必要な分子濃度のパラメータ調整が行われていること、精神疾患・運動障害においては、パラメータ調整に失敗していることが明らかになった。
ドーパミン異常に伴う精神疾患・運動障害の原因解明や治療法開発につながることに期待
今回の知見に基づき、統合失調症、DYT1ジストニアをはじめとするドーパミン異常に伴うさまざまな精神疾患・運動障害の原因の理解が進み、よりよい治療法が開発されることが期待される、と研究グループは述べている。
▼関連リンク
・生理学研究所 プレスリリース



