IL-33はどのような状況で抗腫瘍免疫応答を最大限発揮するのか?
大阪大学は9月9日、サイトカインIL-33が樹状細胞のセマフォリン4Aの発現を誘導し、抗腫瘍免疫を活性化させることを解明したと発表した。この研究は、同大大学院医学系研究科の菅泰彦特任助教(オンコロジーセンター)、熊ノ郷淳教授(呼吸器・免疫内科学)、キャンパスライフ健康支援センターの長友泉教授らの研究グループによるもの。研究成果は、「The Journal of Immunology」に掲載されている。
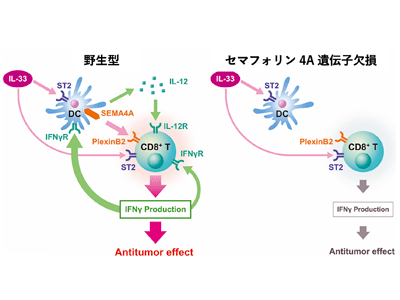
画像はリリースより
免疫チェックポイント阻害剤によるがん免疫療法が、新しい標準的な治療法として確立されつつある。この治療法が有効であるための条件として、自発的な抗腫瘍免疫応答が十分に生じていることが必要と考えられている。しかし、そのような応答が生じていない、あるいは弱い症例では、あまり効果が期待出来ないという弱点がある。有効性を改善するための1つの戦略として、アジュバントやサイトカインによる抗腫瘍免疫応答の促進が挙げられる。
今回、研究グループは、サイトカインの一種であるIL-33に着目。IL-33 は近年、腫瘍に対しての役割が注目されているサイトカインだが、どのような状況で抗腫瘍免疫応答を最大限発揮するのかはいまだ不明だ。
IL-33<樹状細胞刺激<セマフォリン4A発現<CTL刺激<IFNγ産生促進
研究グループは、まず、マウス肺がん細胞株と同系マウスを使用して、IL-33が細胞傷害性T細胞(CTL)によるIFNγ産生を促進し、腫瘍増殖を有意に抑制することを示した。また、セマフォリン4A遺伝子欠損マウスを使用した一連の実験により、腫瘍微小環境に存在する免疫系細胞のセマフォリン4Aの発現が、IL-33の抗腫瘍活性にとって必須であることを証明した。
さらに詳細な解析の結果、IL-33は樹状細胞(DC)に作用して、MyD88シグナルによりセマフォリン4Aの発現を誘導すること、および、そのセマフォリン4Aは、CTLに発現しているレセプターPlexin B2を刺激してIFNγ産生を促進させることを解明した。
逆に、活性化CTLにより分泌されたIFNγがDCを刺激し、DCからIL-12が産生されCTLを刺激することにより、相互に活性化するpositive feedback loopが形成されていることも示した。このような、腫瘍微小環境におけるDCとCTLのIL-33誘導性・セマフォリン4A媒介性の相互活性化メカニズムは、これまでに知られていない新規の機序だ。
マウスで得られたデータを基に臨床応用へ向けて研究推進
今回の研究成果により、IL-33とセマフォリン4Aが治療標的となり得ること、および、DC活性化状態のバイオマーカーとしてもセマフォリン4Aが応用出来る可能性が示唆された。研究グループは、マウスで得られたデータを基に、ヒト肺がん患者においても臨床データやサンプルを用いた解析を行い、これらの臨床応用に向けて更に研究を進めていきたい考えを示している。
▼関連リンク
・大阪大学 ResOU



