検体入手や解析が難しく、発がん機構やゲノム異常がほとんど不明
国立がん研究センターは8月17日、スキルス胃がんについて、腹膜播種による腹水細胞を用いた全ゲノム解析等によって、疾患に特徴的なゲノム異常を解明したと発表した。この研究は、同センター研究所細胞情報学分野の間野博行分野長、基盤的臨床開発研究コアセンター創薬標的・シーズ探索部門の佐々木博己研究員、慶應義塾大学医学部病理学教室の金井弥栄教授らの研究グループによるもの。研究成果は、「Nature Cancer」にオンライン掲載されている。
画像はリリースより
スキルス胃がんは、がん細胞が粘膜下に広く浸潤し、診断時にすでに腹膜播種や腹水をきたすことが多い悪性腫瘍で、膵臓がんなどと並んで最も予後の悪いがん種と考えられている。スキルス胃がんでは腫瘍細胞は低分化型あるいは印環細胞の形態を取り、粘膜下への浸潤によって周辺間質の著明な線維化をきたすことが知られている。これまで胃がん全体あるいはびまん性胃がんのゲノム解析は報告されてきたが、スキルス胃がんは、手術があまり行われず、また検体を入手できても、線維化が強くがん細胞の含有割合が低いため、スキルス胃がんのゲノム異常や発がん機構は、ほとんど明らかにされていなかった。
胃がん患者の腹膜播種による腹水細胞を用いて細胞株樹立、98例を解析
今回研究グループは、高純度の試料を得るため、胃がんの腹膜播種からがん性腹水をきたした患者の腹水中のがん細胞を純化するとともにがん細胞株を樹立し、これら試料に対して全ゲノム解析を含む網羅的マルチオミックス解析を行い、スキルス胃がんの病態解明と治療標的の同定を試みた。
胃がんの腹膜播種により腹水が貯留した患者の同意の下で腹水を採取し、がん細胞を純化するとともに、細胞株の樹立も試みた。その結果、純化がん細胞のみが得られた患者39例、がん細胞株のみ得られた患者22例、両者ともに得られた患者さん37例の、計98例について腹水由来のがん試料が得られた。
これらの試料を同じ患者のペア末梢血とともに、ゲノムDNAを調製し全ゲノム解析を行った。純化がん細胞および細胞株についてはRNAも調製し、次世代シークエンサーによる配列解析も実施した。さらに細胞株が得られた症例については網羅的メチル化解析、網羅的エンハンサー解析などのエピゲノム解析を行い統合的な解釈を試みた。これら症例の約9割は、低分化型がん細胞、印環細胞陽性、びまん性浸潤、最初の転移巣が腹膜、などの特徴を組み合わせて有しており、いわゆるスキルス胃がんに該当すると考えられた。
受容体型チロシンキナーゼ-RAS-MAPK経路で高頻度にがん化変異を確認
全ゲノム解析の結果、興味深いことに、細胞増殖の重要な制御系である受容体型チロシンキナーゼ-RAS-MAPK経路の遺伝子群に高頻度にがん化変異(増幅)が認められた。中でも、10コピー以上の高度増幅が認められた遺伝子としてKRAS(全症例中19.4%)、FGFR2(11.2%)、MET(7.1%)、ERBB2(5.1%)およびEGFR(4.1%)が挙げられる。さらに肺がんで認められるEML4-ALK融合遺伝子が2例、甲状腺がんで認められるAGK-BRAF融合遺伝子が1例で発見された。これら遺伝子の増幅・融合は全体の50%におよび、スキルス胃がんの発症機構に染色体の構造異常が大きな役割を果たしていることが明らかとなった。なおKRAS遺伝子については点突然変異(アミノ酸置換)による活性化も11.2%で認められており、上記の遺伝子高度増幅と相互排他的に存在していた。
これら異常の多くに対応した分子標的治療薬はすでに開発・実用化されている。そこで、EML4-ALK、MET、FGFR2各遺伝子の増幅異常をもつ細胞株をマウス腹腔に接種したのちに、ALK阻害剤(alectinib)、MET阻害剤(capmatinib)、FGFR2阻害剤(infigratinib)をそれぞれ経口投与した結果、腹膜播種が速やかに消失することが確認された。
腹膜播種モデルマウスにTEAD阻害剤投与、がん細胞の増殖抑制
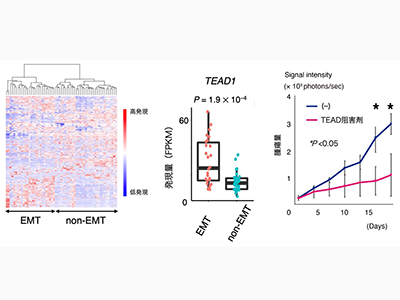
一方、網羅的RNA解析により得られた遺伝子発現プロファイルをもとに検体を階層的クラスタリングすると、全体が大きく2群に分類された。両群を区別している遺伝子を探索したところ、EMTに関与する遺伝子群が最も明瞭に両群を分けることが明らかになった。実際、EMTに重要な役割を果たすTGF-β経路の遺伝子群が発現上昇している「EMTグループ」と、それが認められない「non-EMTグループ」に区別された。
また、興味深いことに、EMTグループ特異的に、細胞増殖および器官のサイズを制御するHippo経路の転写因子群TEAD1、WWTR1(TAZ)などが高発現していたことも確認された。EMT特異的なHippo経路の転写因子高発現はこれまで報告がなかった。そこでTEAD抑制の治療効果を検討するために、EMTグループの細胞株を用いて腹膜播種モデルマウスを作成し、TEAD1-4の阻害剤を経口投与したところ、がん細胞の増殖が抑えられた。またTEAD阻害剤とMAPK経路阻害剤の同時投与によって、さらに強いがん細胞死が誘導された。
がん遺伝子パネル検査への実装や分子標的治療薬の開発への展開に期待
今回の研究成果により、スキルス胃がんの詳細なゲノム異常が明らかになった。特に受容体型チロシンキナーゼ-RAS-MAPK経路の遺伝子の高度増幅が特徴的である。「マウス実験で多くの分子標的薬の有効性も確認されたことから、今後は同様な患者のがん遺伝子パネル検査への実装や分子標的治療薬の開発への展開が期待される。またTEAD経路の阻害が全く新しいスキルス胃がんの治療薬剤として開発される可能性がある」と、研究グループは述べている。
▼関連リンク
・国立がん研究センター プレスリリース






