クローン性造血による予後と遺伝子変異・コピー数異常との関係は?
京都大学は7月9日、クローン性造血の臨床予後への影響を解明したと発表した。この研究は、同大大学院医学研究科腫瘍生物学講座の小川誠司教授(兼、同大高等研究院ヒト生物学高等研究拠点(ASHBi)主任研究者)、佐伯龍之介同博士課程学生、理化学研究所生命医科学研究センター基盤技術開発研究チームの桃沢幸秀チームリーダー、東京大学医科学研究所人癌病因遺伝子分野の村上善則教授、東京医科歯科大学M&Dデータ科学センターの宮野悟センター長(東京大学名誉教授)らを中心とする研究グループによるもの。研究成果は、「Nature Medicine」にオンライン掲載されている。
画像はリリースより
次世代シーケンサーによる大規模な遺伝子解析により、血液がん(急性骨髄性白血病や骨髄異形成症候群)は特定のゲノム異常によって引き起こされることを、同研究グループは過去に報告した。しかし、近年の研究によってゲノム異常は血液がんを発症していない人の血液でも一定の頻度で検出されることが判明し、「クローン性造血」として注目を集めている。クローン性造血は血液がんの前がん病変と考えられているが、興味深いことに動脈硬化の進展にも関わっていることが報告されており、高齢者における主要な予後規定因子として認識され始めている。クローン性造血で検出される主なゲノム異常は、大きく遺伝子変異とコピー数異常の2種類に分類される。しかし、既存の研究で両者は別々に検討されてきたため、クローン性造血における両者の関係性については十分な理解が得られていなかった。
1万人以上の末梢血を解析、クローン性造血の段階から両アリル異常の存在が判明
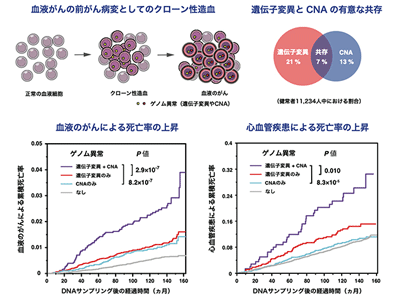
今回、研究グループは、クローン性造血における遺伝子変異とコピー数異常の関係性を明らかにするため、バイオバンク ジャパン (BBJ)に登録された1万1,234人の被験者の末梢血サンプルを用いて、遺伝子変異とコピー数異常の統合解析を実施。その結果、被験者の40%でいずれかの異常が検出された。また、被験者の7%(陽性例の16%)では両方の病変を認め、統計学的に有意な共存を示すことから両者の協調的な関係が示唆された。特に、DNMT3A、TET2、JAK2、TP53などの遺伝子では遺伝子変異とコピー数異常が頻繁に共存し、遺伝子の両アリル異常を来していると考えられた。これらの遺伝子の両アリル異常は血液がんでは既知の所見だが、今回の研究によりクローン性造血の段階から存在することが判明した。
遺伝子変異とコピー数異常は血液がんと心血管疾患のリスクに協調的に作用
血液がんのリスクについては、過去の報告と一致して遺伝子変異あるいはコピー数異常を有する例では有意なリスクの上昇を認めたが、血液がんの中でも骨髄系腫瘍ではリンパ系腫瘍に比べて強いリスクの上昇を認めた。また遺伝子変異とコピー数異常が共存している例では、単独の場合に比べて血液がんによる死亡率が上昇し、両者が協調的に血液がんの発症に関わっていることが示唆された。特に、両者が同一の遺伝子(DNMT3A、TET2、TP53、JAK2など)を標的として両アリル異常を起こしている場合には、さらにリスクが上昇することがわかった。
心血管疾患については、既存の報告の通り遺伝子変異が検出された例では有意にリスクが上昇していた。加えて、遺伝子変異が検出された例では高血圧を高頻度に認め、クローン性造血が動脈硬化を促進するという定説をさらにサポートする結果となった。また、遺伝子変異とコピー数異常が共存する例では、単独の場合に比べて心血管疾患による死亡率が上昇し、心血管疾患の発症についても2種類の病変が協調的に作用していることが類推された。
これらの結果から、遺伝子変異とコピー数異常は血液がんと心血管疾患のリスクに協調的に作用していて、クローン性造血について正確な理解を得るためには両者を統合的に評価することが重要であると考えられた。研究グループは今回の成果について、「血液がんの起源を理解するための手がかりを与えるのみならず、クローン性造血に基づく臨床予後の予測を実現する上で重要な指標となることが期待される」と、述べている。
▼関連リンク
・京都大学 最新の研究成果を知る




