特定臓器を狙い撃ちできるナノカプセルの論理的な設計手法は未確立
北海道大学は6月24日、肺に対して選択的に遺伝子送達可能なナノカプセルの開発に成功したと発表した。この研究は、同大大学院薬学研究院の原島秀吉教授、佐藤悠介助教および同工学研究院の佐藤敏文教授、磯野拓也准教授らの共同研究グループによるもの。研究成果は、「Materials Horizons」にオンライン掲載されている。
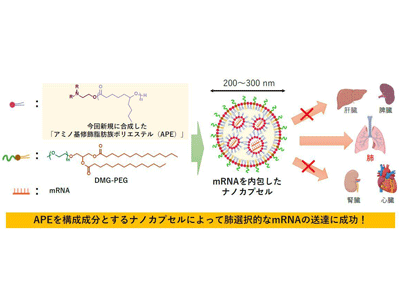
画像はリリースより
mRNAなどの核酸を治療薬とする核酸医薬は、従来医薬品では治療が困難だったさまざまな遺伝子疾患を根治できる可能性を秘めており、低分子医薬と抗体医薬に次ぐ第三の医薬品として近年大きな注目を集めている。新型コロナウイルスに対するmRNAワクチンも核酸医薬の一種。核酸医薬をさまざまな疾病の治療に用いるためには、治療薬本体となる核酸を目的患部に効率的かつ選択的に送り届ける技術の開発が不可欠となる。こうした技術の1つとして、脂質で核酸を包み込んでナノカプセル化する手法が広く利用されている。
例えば、2018年に上市されたONPATTROはsiRNAを脂質でナノカプセル化したものであり、世界初の全身投与型の核酸ナノ医薬として知られている。ONPATTROは血中投与後に速やかに肝臓へ集積し、肝臓において高い治療効果を発現する。一方、肝臓以外の臓器をターゲットとした核酸医薬は非常に少なく、これを可能にするナノカプセルの開発は非常に重要な課題となっている。しかし、特定の臓器を狙い撃ちできるナノカプセルの論理的な設計手法は今のところ確立されておらず、核酸医薬の普及において大きなハードルとなっている。例えば肺疾患は、肺がん、嚢胞性繊維症、肺高血圧症、肺繊維症など多岐にわたり、肺への選択的な核酸送達は臨床上きわめて大きな意味を持つ。
mRNAを肺に高効率で送達できるナノカプセル作製に成功、マウスで確認
研究グループは今回、APEを構成要素とするナノカプセルがmRNAを肺へ選択的に送達できることを見出した。先行研究の結果などからアミノ基で修飾した脂肪族ポリエステル(APE)がナノカプセルの構成要素として有効と考え、分子構造が少しずつ異なる3種類以上ものAPEを候補材料として新規に合成した。新規APEはε-デカラクトンの開環重合によって一段階で容易に得ることができた。
このAPEと補助脂質(既製品のDMG-PEG)で構成されるナノカプセルに緑色蛍光タンパク質をコードするmRNAを封入し、核酸医薬のモデルを調製。マウス個体に対して各ナノカプセルを静脈内投与し、緑色蛍光タンパク質の発現を指標として各臓器へのmRNA送達効率を調査した。その結果、候補材料のうちいくつかが、肺に対して非常に高い効率でmRNAを送達できることを発見した。
APEは市販試薬から一段階で合成可能
従来の脂質のみからなるナノカプセルの場合、血中投与すると肝臓で捕捉されてしまうことが多く、他の臓器へ核酸を送達することは非常に難しいとされていた。また、特定の臓器に対して選択的な送達を実現するためには、標的化リガンドと呼ばれる特別な仕組みをナノカプセルに導入する必要があると考えられていた。
これに対して、今回開発したナノカプセルは標的化リガンドが無いにもかかわらず肺選択的な核酸送達能を示しており、APEは核酸を包み込むナノカプセルとして働くだけでなく、肺に対する標的化リガンドとしての機能も果たすことが判明した。APEは市販の試薬から一段階の合成反応で得ることができ、コスト面でも大変優れている。論文発表に先立ち、このナノカプセルに関する特許を同大から申請しているという。
さまざまな肺疾患への治療応用に期待
今回開発した核酸内包ナノカプセルを活用して、さまざまな肺疾病に対する治療法の確立が期待できる。現状では、APEからなるナノカプセルがどのようなメカニズムで肺選択性を発現しているか不明だが、これを明らかにすることができれば肝臓以外のさまざまな臓器をターゲットとした核酸医薬の開発につながると考えられる。「ONPATTOROや新型コロナウイルスワクチンをはじめとして、核酸医薬はここ最近になって急速に実用化が進められている分野であり、本研究成果は核酸医薬の研究開発を一層後押しするものと期待される」と、研究グループは述べている。
▼関連リンク
・北海道大学 プレスリリース



