胎児期・脳内神経幹細胞でのDNA損傷が出生後の早期神経細胞死を誘発、マウスで確認
東京医科歯科大学は6月14日、前頭側頭葉変性症において、胎児期の脳内の神経幹細胞で起きるDNA損傷が出生後の早期神経細胞死を誘発し病態進展の鍵を握ること、この細胞死を標的とする治療法の可能性を実験的に示したと発表した。この研究は、同大難治疾患研究所/脳統合機能研究センター神経病理学分野の岡澤均教授ら、東邦大学、名古屋市立大学、名古屋大学、東北医科薬科大学、東北大学、東京大学、東京都健康長寿医療センター、京都大学iPS細胞研究所の研究グループによるもの。研究成果は、「Life Science Alliance」オンライン版に掲載されている。
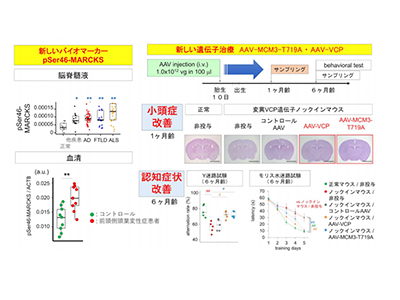
画像はリリースより
前頭側頭葉変性症はアルツハイマー病、レビー小体型認知症に次ぐ有病率を示す認知症のひとつ。細胞内にタウ、TDP43などの異常タンパク質が蓄積・凝集することで病理学的に診断される。前頭側頭葉変性症には、遺伝性の明瞭な家族性前頭側頭葉変性症と、遺伝性の不明瞭な弧発性前頭側頭葉変性症があり、VCP遺伝子、PGRN遺伝子、CHMP2B遺伝子、TDP43遺伝子などが、家族性前頭側頭葉変性症の代表的原因遺伝子として知られている。これらの遺伝子から産生されるタンパク質は、種々の機能を持っているが、いずれもDNA損傷の修復に重要な役割を果たすことで共通している。
研究グループは先行研究により、ハンチントン病や脊髄小脳失調症1型を含む複数の神経変性疾患において、損傷DNAに対する修復機能の低下が神経変性疾患における共通の病態であることを、世界に先駆けて報告してきた。その結果、DNA修復機能低下が、神経変性疾患の共通病態として認められている。前頭側頭葉変性症においても、DNA損傷修復不全が病態に関わる可能性があるが、詳細は明らかではない。また、研究グループが、最近、アルツハイマー病態で明らかにしたような超早期病態(凝集タンパク質の出現前に始まる病態)が存在するかどうかについても、明確な結論は出ていない。
モデルマウス4種、胎児期~成体に至る経過を詳細に調査
今回の研究では、前頭側頭葉変性症の新しいモデルマウス(KIマウス)を4種類用いて、その胎児期から成体に至る経過を詳細に調査。特に、最新のプロテオーム解析法を用いて、胎児期の脳組織中のタンパク質変化を網羅的に調べた。
そして、検出されたタンパク質変化が出生後のモデルマウスの病態とどのように関わるかを調べ、さらに、患者から提供された剖検脳を用いて、モデルマウスで推定された新規病態を確認した。
超早期神経細胞ネクローシス→変性タンパク質凝集への過程、どのタイプの前頭側頭葉変性症でも共通
研究の結果、胎児期神経幹細胞のDNA損傷が十分に修復されないために、誘導されるDNA損傷ストレスが超早期(タンパク質凝集が認められる遥か以前)に前頭側頭葉変性症病態の端緒となること、神経幹細胞に蓄積したDNA損傷は、神経幹細胞から神経細胞に分化した後にも持ち越されて、超早期の神経細胞のネクローシスにつながることがわかった。
前頭側頭葉変性症は、種々の原因遺伝子変異によって発症する多様な疾患グループだ。それにも関わらず、神経幹細胞のDNA損傷から、超早期神経細胞ネクローシスを経て、変性タンパク質凝集につながる過程は、どのタイプの前頭側頭葉変性症においても共通していることが判明した。
超早期神経細胞ネクローシスに対応して、pSer46MARCKSが脳内増
続いて、前頭側頭葉変性症の4種類のKIマウスは、発達期に脳が全体的に小さい小頭症を示し、しかも、成体になるにしたがって、脳のサイズが正常化することがわかった。
また、超早期神経細胞ネクローシスに対応して、リン酸化タンパク質pSer46MARCKSが脳内で増加。これは、モデルマウスのみならず前頭側頭葉変性症ヒト患者の血清でも上昇が検出でき、脳内の神経細胞死を反映するバイオマーカーとして開発できる可能性があることが明らかになった。
前頭側頭葉変性症に対して、ウイルスベクターAAV-MCM3、AAV-VCPなどによる新たな治療法を開発できる可能性がある、としている。
前頭側頭葉変性症発症後の遺伝子治療など、今後開発の可能性も
同研究によって明らかになった超早期病態の神経細胞死(TRIAD)は、研究グループが最近報告したアルツハイマー病の超早期細胞死と同一のものと考えられる。Ser46リン酸化MARCKS増加は、前頭側頭葉変性症患者の脳脊髄液さらに血清においても検出され、バイオマーカーとして開発可能であることが明らかになった。
孤発性前頭側頭葉認知症の患者の剖検脳においても、同様にTRIAD型の神経細胞死が確認できたことから、TRIADは超早期から終末期にかけて持続して発生していることが示唆される。
また、研究グループは、遺伝子治療が前頭側頭葉変性症モデルマウスの認知症状を改善することを明らかにした。論文中では、発症前に遺伝子治療のためのAAVベクターを投与しているが、今後、前頭側頭葉変性症の発症後の遺伝子治療、さらには、その他の治療法(特願 2020-204343)の開発の可能性があると考えられる、と研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース



