「BRCAの機能が正常か否か」しか治療予測の手段がない
東京都立大学は6月8日、XRCC1タンパク質の機能がPARP阻害薬の治療効果に決定的な影響を及ぼすことを明らかにしたと発表した。この研究は、同大理学研究科の廣田耕志教授と京都大学大学院医学研究科の武田俊一教授、サセックス大学のKeith W Caldecott教授らの研究グループによるもの。研究成果は「Molecular Cell」オンライン版に掲載されている。
画像はリリースより
DNAは細胞内で代謝反応物などの影響で毎日多数のDNA損傷を受けている。DNA損傷の中でも、特に塩基の損傷は最も頻繁に見られ、その修復は生き物にとって重要である。DNAやその損傷の修復酵素は、抗がん治療の標的でもある。このような損傷の修復には塩基除去修復が機能することが解明され、2015年にはノーベル化学賞の対象となった。この修復機構は酵母からヒトまで保存されたユニバーサルな機構で、ヒトを含む動物細胞ではPoly[ADP ribose]polymerase(PARP)とXRCC1と呼ばれるタンパク質が新たに修復のコーディネーターとして機能している。PARPはDNA損傷のセンサーとして働き損傷箇所に印をつける。その後、XRCC1が修復に関与するタンパク質群を動員させることで、損傷が修復されることが知られている。
これまでに、さまざまなPARP阻害薬が開発され、これらの薬品はBRCA遺伝子変異陽性の遺伝性乳がん・卵巣がん症候群の治療薬として使用されている。これらの治療薬はPARPの活性を阻害してDNA損傷に結合したPARPの解離を阻害し、PARPが切れたDNA末端に結合した構造をもつ「PARPトラップ」と呼ばれる有毒な中間体を安定化・蓄積させることで、がん細胞を殺傷して増殖を抑える。抗がん剤は一般に副作用が強いために、治療開始前にその治療効果を予測することが望ましいが、BRCAタンパク質の機能が正常か否かのみしか治療予測の手段がなかったことが課題だった。
XRCC1はPARPトラップの解消における因子、PARP阻害薬の治療効果を決定する可能性
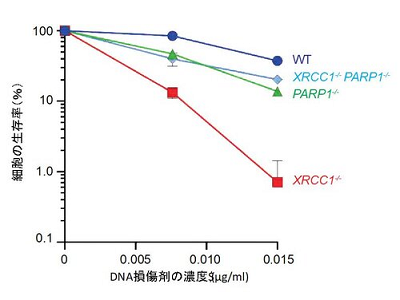
廣田教授と武田教授は、DNA損傷に対するPARPとXRCC1の動きについて詳細に解析した。その結果、ゲノム編集技術でXRCC1遺伝子を欠損させた細胞は、DNA損傷剤に対し大きく細胞生存率の低下を示した。一方、PARPを欠損させた細胞はXRCC1欠損細胞ほど大きな細胞生存率の低下は示さなかった。興味深いことに、XRCC1欠損細胞からPARPをさらに欠損させた二重欠損細胞では、大幅な細胞生存率の回復が見られ、PARP単独欠損と同程度の生存率を示した。
この発見は、これまでPARPとXRCC1がいつも一緒に損傷修復に寄与するという教科書的なドグマを覆すほど意外な発見であるとともに、PARPが有毒な効果を細胞内で発揮していて、XRCC1がこの毒性を抑えていることを示している。さらに、XRCC1欠損細胞では有毒なPARPトラップがPARP阻害薬を投与していない状況でも大量に蓄積していることも発見した。
これらの結果から、XRCC1がPARPトラップの解消における決定的因子であることが示されるとともに、遺伝性乳がん・卵巣がん症候群の治療に用いられるPARP阻害薬の治療効果の決定因子となることが示唆された。
XRCC1遺伝子の状況に基づいた新規治療開発などに期待
研究グループは、今回の研究成果の意義、波及効果について、次のように考察している。
XRCC1遺伝子の発現低下や変異による活性低下を示すがん細胞では、PARPトラップの解消が不良となっていることが予想される。XRCC1遺伝子のがん細胞での状況(発現や変異)について治療前に診断し、XRCC1遺伝子変異(または機能低下)の細胞にもBRCA遺伝子変異陽性乳がんの治療にすでに用いられているさまざまなPARP阻害薬が有効であると推定される。このようなXRCC1遺伝子の状況に基づいた治療につながることが期待される。
また、XRCC1欠損細胞ではDNA損傷剤(DNAのメチル化など誘導)に高い感受性を示すことから、従来の脳腫瘍の治療に用いられているDNAメチル化薬品等がXRCC1遺伝子変異(または機能低下)をもつがん細胞の治療に有効である可能性が高い。これらのPARP阻害薬やDNAメチル化薬品等の間のXRCC1変異とのシナジー効果について今後検討されることが期待される。
さらに、XRCC1の機能低下は大幅なPARP阻害薬に対する増感作用が見込まれる。XRCC1をターゲットとした薬品を開発できれば、既存のPARP阻害薬を大幅に増感でき、BRCA遺伝子変異陽性乳がん以外の広範ながん治療への応用も見込まれる。XRCC1は、治療前に治療効果を予測するバイオマーカーとして利用し得ることも考えられる。
PARP阻害薬の問題は、治療開始直後に非常に有効であるが、その後にPARP阻害薬耐性のがんが再発することである。今回の研究成果は、上記にように、治療効果の予測や新規の抗がん剤開発などの応用研究に結びつくことや、再発機構の解明に役立つことが期待されると、研究グループは述べている。
▼関連リンク
・東京都立大学 ニュース




