ASXL1の機能異常とCHの因果関係をマウスモデルで解析
東京大学医科学研究所は5月11日、造血系の加齢に伴うクローン性造血(Clonal hematopoiesis:CH)の成り立ちと、それが血液がんへ進展するメカニズムについて、ASXL1変異を有するマウスモデルを用いて明らかにしたと発表した。この研究は、同研究所細胞療法分野の北村俊雄教授と東京大学大学院新領域創成科学研究科の合山進教授らの研究グループによるもの。研究成果は、「Nature Communications」(オンライン版)に掲載されている。
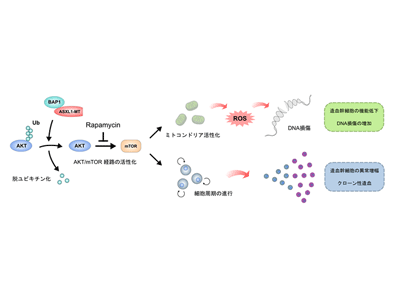
画像はリリースより
血液学的な異常が認められない健常な高齢者においても、体細胞変異を伴ったクローナルな造血が起こり、造血器腫瘍の発症リスクが上昇することが知られている。このような現象はCHと呼ばれ、血液疾患に限らず、心筋梗塞や脳梗塞のような血管病変のリスクも上昇させることから、その進展機序の解明は喫緊の課題となっている。
CHではDNMT3A、TET2、ASXL1を含むヒストン修飾因子の変異が高頻度に同定される。DNMT3AおよびTET2欠失マウスの解析により、これらの変異を有する造血幹細胞では自己複製能が亢進し、造血細胞のクローナルな増殖が起こると考えられている。一方、ASXL1変異を有するマウスモデルでは、造血幹細胞の機能はむしろ低下することが示されており、ASXL1の機能異常とCHの因果関係は解明されていなかった。
変異型ASXL1は機能低下した異常な造血幹細胞を加齢に伴い増加
そこで今回、研究グループは、変異型ASXL1(ASXL1-MT)を発現するノックイン(KI)マウスの解析を通じ、ASXL1変異がCHを惹起する分子機序の解明を試みた。若齢(12週)のASXL1-MT KIマウスでは、血液学的な異常は認められず、造血器腫瘍も発症しなかった。骨髄中の造血幹細胞は減少し、既報と同様に移植後の骨髄再構築能は低下していた。
次に、CHの頻度は加齢に伴って増加することから、生後約2年が経過した高齢マウスの解析を実施。すると、加齢したASXL1-MT KIマウスは、造血器腫瘍を発症しないものの、白血球の減少と貧血の進行が認められた。若齢マウスとは対照的に、造血幹細胞は顕著に増加していたが、その骨髄再構築能は低下していた。
さらに、ヒトで起こるCHにより近い条件でASXL1変異の影響を検討するため、Mx1-CreトランスジェニックマウスとASXL1-MT KIマウスを交配し、ASXL1-MTをモザイクに発現するマウスを確立した。18か月の観察期間において、ASXL1-MT発現細胞は経時的に増加し、最終的に造血幹細胞分画を占拠するに至った。これらの結果から、ASXL1-MTは機能が低下した異常な造血幹細胞を加齢に伴って増加させ、その集団を拡大させることが明らかとなった。
変異型ASXL1による造血幹細胞機能異常の主な原因はAKT/mTOR経路の活性化
以上の病態を説明するメカニズムとして、ASXL1-MTが脱ユビキチン化酵素であるBAP1と協調し、AKTを脱ユビキチン化することが明らかとなった。安定化したAKTはAKT/mTOR経路を活性化し、造血幹細胞の細胞周期の進行とその増殖を促進した。一方、活性化したAKT/mTOR経路はミトコンドリアでの代謝亢進、活性酸素の増加、そしてDNA損傷の増加を引き起こした。これは造血幹細胞の機能を低下させるだけでなく、ASXL1の変異自体が新たな遺伝子変異を惹起し、悪性化に寄与することを示唆する所見だという。
mTOR阻害薬であるラパマイシンを高齢マウスに投与すると、造血幹細胞の細胞周期は静止期に戻り、異常な増殖は抑制された。さらに、ミトコンドリアの活性化、活性酸素の増加、DNA損傷の増加、そして造血再構築能の低下はすべてレスキューされた。したがって、AKT/mTOR経路の活性化は、ASXL1-MTによる造血幹細胞の機能異常の主要な原因であることが明らかになった。
今回の研究により、ASXL1変異は造血再構築能の欠如した異常な造血幹細胞を増殖させることで、CHを引き起こすことが示唆された。本来、ASXL1-MTはヒストン修飾を変化させることでその作用を発揮すると考えられてきたが、それに加えてシグナル伝達経路に直接作用することで、病態形成に寄与することが明らかになった。「今回の研究結果は、ASXL1変異を有するCHが治療可能な病態である可能性を示唆しており、造血器腫瘍の予防的治療に道が開かれることが期待される」と、研究グループは述べている。
▼関連リンク
・東京大学医科学研究所 プレスリリース




