体内時計は生物種ごとに独立進化したと考えられていた
東京大学は5月1日、哺乳類、昆虫、植物および細菌の体内時計に共通して働く因子として、カルシウムイオン(Ca2+)制御タンパク質であるNa+/Ca2+交換輸送体(NCX)を発見したと発表した。この研究は、名古屋大学トランスフォーマティブ生命分子研究所の金尚宏特任講師(研究当時:東京大学大学院理学系研究科特任助教)、東京大学大学院理学系研究科生物科学専攻の深田吉孝教授(研究当時)、福岡大学医学部薬理学の岩本隆宏教授らの研究グループによるもの。研究成果は、「Science Advances」に掲載されている。
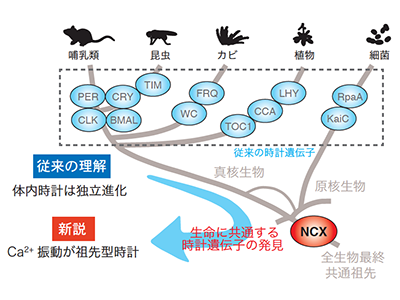
画像はリリースより
体内時計の仕組みの理解は、睡眠障害やうつ病の克服など臨床的な応用に直結しており、注目を集めている。24時間周期の体内時計は概日時計と呼ばれ、ヒトからバクテリアまで存在している。概日時計によって生み出される1日周期のリズムは概日リズムと呼ばれ、時計遺伝子による転写・翻訳フィードバックループ(以下、転写ループ)が重要な役割を果たしている。これまで、時計遺伝子は動物、真菌類、植物、細菌で見つかっているが、それらの間で相同性が低いことから、生物種ごとに独立進化したと考えられてきた。
時計遺伝子による転写ループが概日リズム生成に必須であることはわかっていたが、概日時計の本体と考えるには不思議な部分があった。概日時計は温度補償性という、環境温度が変化しても周期が24時間に保たれる性質を有する。転写や翻訳などの生化学反応は、温度によって反応速度が変化し、例えば温度を10度下げると、その反応速度は1/2倍から1/3倍に遅くなってしまう。そこで、単純に転写ループだけで体内時計が構成されているとすると、温度が10度下がった場合に時計の周期が48時間や72時間となってしまう。温度補償性を説明するためには、温度低下による生化学反応の速度低下を補償する仕組みが必要であることが70年近く前から提唱されていたが、その実体は明らかにされていなかった。
細胞内Ca2+振動が転写ループの上流で機能する祖先的な振動体である可能性
研究グループは今回、培養細胞にも概日時計が存在するという性質に着目し、細胞時計の温度補償性に影響を及ぼす薬剤をスクリーニングした。その結果、Na+/Ca2+交換輸送体(NCX)とCa2+/カルモジュリン依存性キナーゼII(CaMKII)という、細胞内カルシウムシグナルに関わる2つのタンパク質の阻害剤存在下では、温度補償性が破綻することを見出した。
解析の結果、環境温度の低下に伴ってNCXが細胞内Ca2+流入を促進し、それによって活性化したCaMKIIが転写ループの振動速度の低下を防いでいることがわかった。つまり、本来は温度低下によって速度低下する転写ループは、低温で活性化するCa2+シグナルによって24時間の周期に保たれていたのである。この低温性Ca2+シグナルは哺乳類だけでなく昆虫、植物、細菌の概日時計でも機能していることが判明し、幅広い生命に保存された仕組みであることがわかった。NCXの機能が広い生物種の時計機能に保存されているという事実は、NCXがこれらの共通祖先の時計機能に関わっていたことを示唆する。つまり、時計遺伝子の転写ループは動物や植物、細菌が系統的に分岐した後に生まれた一方で、カルシウムによる概日時計の制御は共通祖先から機能していたと考えられるという。
研究グループはさらに、NCXが温度補償性だけでなく概日時計そのものにも関わると推定し、NCX機能が低下した動物を解析した。その結果、マウスおよびショウジョウバエにおいて、1日周期の行動リズムが著しく障害されることがわかった。これらの動物の体内時計のペースメーカー神経において、細胞内Ca2+は1日周期で増減を繰り返していたことから、細胞内Ca2+振動が転写ループの上流で機能する祖先的な振動体なのではないかとの見解に至ったという。
睡眠障害やうつ病など、体内時計に関わる疾患克服の技術開発に期待
現在の生命は、全生物最終共通祖先(Last Universal Common Ancestor:LUCA)から多様化し進化して生まれたと考えられている。そこで、現生の生物において広く保存された遺伝子群を調べれば、LUCAが保持していたであろう遺伝子が予測される。2016年にドイツの研究者らは細菌と古細菌の間で高度に保存された355の遺伝子を同定し、それらをLUCAの遺伝子群と結論した。今回の研究で見つかったNCXをコードする遺伝子は、その355の遺伝子群に含まれている。このことから、体内時計の起源はこれまで考えられていたよりもずっと古く、LUCAが存在した時代である約38億年前から存在した可能性も考えられるという。同研究成果は、生命の共通祖先において、どのようにして体内時計が生まれたのかを知る画期的な手がかりとなったと言える。
共通祖先の体内時計の仕組みは、現生の生物でも中心的な役割を保持している。研究グループは、NCXやCaMKII阻害剤を用いることで、概日時計の周期や時刻を制御することに成功している。「これらの発見は、細胞内Ca2+の制御によって体内時計を自由に制御できる技術開発につながるものであり、睡眠障害やうつ病など、体内時計に関わる疾患の克服へ新しい道を切り開いたと言える」と、研究グループは述べている。
▼関連リンク
・東京大学大学院理学系研究科・理学部 プレスリリース




