新規のHSC維持機構とThpo受容体作動薬の作用機構を明らかに
東京女子医科大学は4月6日、造血幹細胞の幹細胞能制御の新たなメカニズムを解明したと発表した。この研究は、同大顕微解剖形態形成分野の石津綾子らのグループと、シンガポール国立大学がん科学研究所および熊本大学国際先端医学研究機構の須田年生教授らの研究グループとの共同研究グループによるもの。研究成果は、「Blood」に掲載されている。
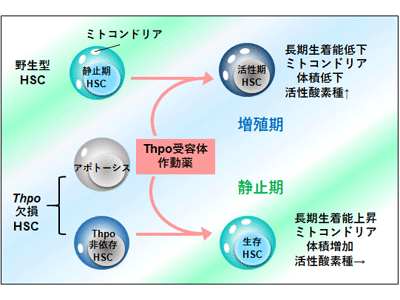
画像はリリースより
一生涯にわたる恒常的な血球産生には、造血幹細胞(hematopoietic stem cell:HSC)の維持・増殖・分化が不可欠だ。しかし、HSCの維持・増殖・分化がどのように制御されているのか、いまだその全容は解明されていない。成人期HSCはストレス造血時などに備え、自己複製能を保持し細胞周期静止期状態で維持されている。1個体において、一つのHSCは最小限の増殖回数しか経験せず、特にミトコンドリア代謝活性を抑制し、低酸素下で解糖系代謝に依存することが、HSCの少ない増殖回数、静止期性の維持に関連するものと考えられている。
一方、HSCに直接作用し、その静止期、分化などの機能を調整する数少ないサイトカインの一つにThrombopoietin(Thpo)がある。ThpoはHSCの静止期を維持するとともに、自己複製増殖も活性化する一見矛盾した作用機構が報告されている。研究グループは今回、ThpoによるHSC静止期誘導とミトコンドリア活性に焦点を当て、新規のHSC維持機構とThpo受容体作動薬の作用機構を新たに報告した。
造血幹細胞の増幅とともに静止性の誘導を確認、Thpo欠損下でも生存できる造血幹細胞のサブグループがある可能性
Thpoは巨核球・血小板産生のみならず、HSCの自己複製増殖を引き起こすことが知られている。一方、成人期のThpo遺伝子欠損マウスやThpo受容体であるMpl遺伝子欠損マウスにおいて、Thpoシグナルの活性化はHSCの静止性の維持と同時に自己複製の促進を行うことも報告されている。
今回の研究では、独自に開発したThpo遺伝子欠損マウスの成人期骨髄HSCは、過去の報告と同様にHSC静止期の減少が認められたが、細胞周期の詳細な解析により、Thpo遺伝子欠損マウス由来HSCではSubG1期の頻度の有意な上昇がみられ、Annexin V染色性の上昇もみられたため、アポトーシス誘導が促進することを確認した。
また、Thpo作動薬のRomiplostimをThpo遺伝子欠損マウスと野生型マウスに連日投与したところ、野生型マウスではRomiplostim投与とともに増殖期HSCのみの増加が認められたが、Thpo遺伝子欠損マウスでは増殖期ではなく静止期にあるHSC数の増加がみられた。さらに遺伝子発現解析や種々の代謝解析を行ったところ、Thpo欠損HSCは、ミトコンドリア代謝、オートファジー、タンパク産生など広く代謝に関わる変動が認められ、静止性を獲得する際にこれらの正常化が認められることが確認された。これらの結果は、HSCの静止性の維持にはThpoによる代謝調整が重要であり、また、Thpo非依存性に生存し、Thpoシグナルに異なった反応性を示すHSCが骨髄内に存在することを示唆していたという。
HSCのThpo反応性のさらなる解明が、造血疾患の病態解明と治療法開発につながることに期待
近年、HSCは遺伝子発現、タンパク発現などにおいて多様性(heterogeneity)を有し、分化・増殖・維持機能も異なった集団からできていると考えられている。今回の研究では、Thpo反応性においてのHSC Heterogeneityが明確化され、Thpo反応性がHSCの静止状態の維持と、それにかかわる代謝状態を制御することが明らかになった。
治療目的で、生体外でのHSC培養・維持法が検証されているものの、幹細胞能の高いHSCを生体内外で維持する方法は確立されていない。「本研究をさらに発展させ、治療応用を目的とした生体内外のHSC増幅と維持の新規方法を開拓し、効率化を目指していきたいと考えている。また、Thpo作動薬の使用は既存治療で効果不十分な再生不良性貧血患者の適応として認可されており、今後、HSCのThpo反応性のさらなる解明は、造血疾患の病態解明と治療開発につながると思われる」と、研究グループは述べている。
▼関連リンク
・東京女子医科大学 お知らせ




