カスタムパネル解析で陰性の6症例対象、全エクソームのトリオ解析を実施
東京医科歯科大学は3月18日、小頭症および低身長の新規原因遺伝子として、動原体の構成要素であるNUF2遺伝子を同定したと発表した。この研究は、同大難治疾患研究所分子細胞遺伝分野のDaniela Tiaki Uehara特任助教、稲澤譲治教授と熊本大学附属病院新生児学寄付講座の三渕浩特任教授らの研究グループによるもの。研究成果は、国際科学雑誌「Human Genetics」オンライン版に掲載されている。
画像はリリースより
研究グループは、2005年から全国23の小児医療施設とコンソーシアムを形成し、診断未確定の多発奇形(multiple congenital anomalies:MCA)を伴う発達遅滞(intellectual disability:ID)645症例を対象として、その原因の探索を行ってきた。その結果、これまでに、24%(155/645)に病因性のコピー数変化(copy number variant:CNV)を検出。次に、病因性CNVが陰性の104症例を対象に、すでにID/MCAの原因遺伝子と報告されている75種類を含むカスタムパネルを用いた遺伝子変異解析を行い、19%(20/104)に病因性と判断される点変異(single nucleotide variant:SNV)を検出した。
さらに、カスタムパネル解析で陰性の6症例を対象に全エクソームのトリオ解析を行い、小頭症および低身長の新規原因遺伝子として、動原体の構成要素であるNUF2遺伝子を同定した。
小頭症、低身長などを呈する14歳男児で同定
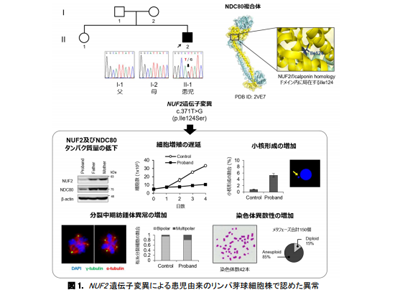
今回、小頭症、低身長、両側声帯まひ、耳介低位、心房中隔欠損症などを呈する14歳の男児において、トリオ全エクソーム解析から、de novoで生じたNUF2遺伝子のヘテロ接合性ミスセンス変異(c.371T>G, p.Ile124Ser)を同定した。
NUF2(NUF2 component of NDC80 kinetochore complex)は、動原体のヘテロ四量体であるNDC80複合体(NUF2、NDC80、SPC24、SPC25)のタンパク質構成要素の一つをコードする遺伝子。特に、NUF2はNDC80と複合体を形成し、微小管と直接に結合することにより染色体分裂および紡錘体形成チェックポイントを制御する。Ile124アミノ酸残基は、NUF2のN末端のcalponin homology(CH)ドメインに局在し、NDC80のCHドメインと相互作用する。
p.Ile124Ser変異は、NUF2のCHドメインで疎水性相互作用の喪失を引き起こし、NDC80-NUF2 複合体の安定性を阻害すると予測された。患児由来の不死化リンパ芽球細胞株を用いたin vitro 実験より、NUF2およびNDC80の両タンパク質量の低下が確認された。また、NUF2とNDC80の減少により、患児由来の細胞では染色体異数性、小核形成の増加、細胞増殖の遅延、紡錘体の異常などが認められた。それらの異常は、胎児脳の発達において小頭症の発症に関連している可能性が示唆された。
NUF2変異の追加症例集積により、小頭症との病態関連性など解明に期待
長らく診断未確定の状態であった同症例において、小頭症および低身長の新規原因遺伝子のNUF2が同定された。また、NUF2における変異がNDC80-NUF2複合体の相互制御に重要な影響を及ぼすことが明らかになった。さらに、NDC80複合体を構成する遺伝子の病因性変異は、今回の報告が初めての例となる。
今回、患者と家族の十数年間の長期にわたる協力によって原因が明らかになり、患者の今後のライフステージにおいても、有用なアドバイスが可能となった。さらに今後、NUF2変異を持つ追加の症例が集積されることにより、小頭症との病態関連性や発症機構がより詳細に明らかにされ、適切な医療、福祉、教育に寄与することが期待される、と研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース



