AAVベクターに利用できる抑制性ニューロン特異的なGAD65プロモーターを新規開発
群馬大学は3月17日、遺伝子治療用に利用されるアデノ随伴ウイルス(AAV)ベクターを用いて、脳の抑制性ニューロンだけに外来遺伝子を発現させる手法を開発したと発表した。この研究は、同大医学部医学科6年生の星野千秋氏、医学系研究科の今野歩講師、細井延武准教授、および未来先端研究機構の平井宏和教授らの研究グループと、大阪大学大学院生命機能研究科、群馬大学眼科学教室および東北大学大学院歯学研究科口腔生理学分野の共同研究グループによるもの。研究成果は、「Molecular Brain」電子版に掲載されている。
画像はリリースより
ニューロンにはさまざまな種類があるが、大きく興奮性ニューロンと抑制性ニューロンに分けることができる。興奮性ニューロンが作る神経回路に抑制性ニューロンが組み込まれ、ネットワークを制御することで、複雑な脳機能の実現が可能となる。脳神経研究の多くは、マウスを使って行われるが、近年、生後~成熟後のマウスに遺伝子導入を行う際、AAVベクターがよく利用される。
研究グループは、このAAVベクターに利用できる抑制性ニューロン特異的なGAD65プロモーターを新規に開発した。GAD65は、抑制性ニューロンにおいて抑制性ニューロンの神経伝達物質であるGABAをグルタミン酸から合成する酵素。GAD65の遺伝子は全ての細胞に存在するが、抑制性ニューロンだけでGAD遺伝子が転写・翻訳される。そこでGAD遺伝子の上流域から、抑制性ニューロンだけで発現を誘導する部分をスクリーニングし、「GAD65プロモーター」と命名した。
AAVベクターの静脈投与のみで全脳領域の抑制性ニューロンへ選択的な遺伝子発現が可能
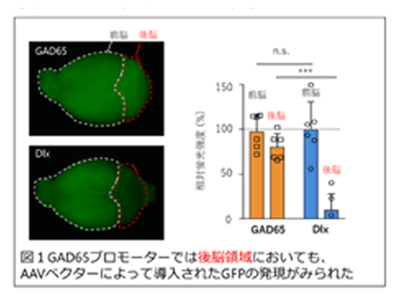
これまでAAVベクターを用いて、抑制性ニューロン選択的に遺伝子を発現させる手段としては、Dlxエンハンサー(以下Dlx)が存在していたが、前脳領域における抑制性ニューロンに対してのみ有効だった。
今回研究グループはGAD65プロモーターの発現特性を調べるために、血液脳関門透過型AAVベクター(AAV-PHP.B)を経静脈的に投与し、全脳領域での遺伝子発現パターンを解析。その結果、GAD65プロモーターは前脳のみならず、後脳を含む全脳領域において、遺伝子発現をもたらすことが明らかになった。さらに、すべての抑制性ニューロンにtdTomato(赤色蛍光タンパク質)が発現しているVGAT-tdTomatoマウスを用いて、GAD65プロモーターの特異性を検討したところ、95%以上の高い特異性で抑制性ニューロン選択的な遺伝子発現が起きていることが明らかとなった。
抑制性ニューロンが関与する精神疾患などの研究推進へ
今回の研究成果により、マウス全脳域の抑制性ニューロンに対して、高い特異性で目的遺伝子を発現させることが可能となった。また同研究グループは最近、このような細胞種特異的プロモーターと人工miRNAをAAVベクターに組み込むことにより、細胞種特異的な遺伝子ノックダウンが可能であることも報告しており、今回報告されたGAD65プロモーターでも、同様の方法が使えると考えられる。
抑制性ニューロンの機能不全は統合失調症をはじめとする種々の精神疾患との関連が指摘されている。このような根本的な治療法のない疾患において、基礎的な研究を推進することは必要不可欠だ。今後、今回の手法を脳の疾患の基礎研究に応用し、新たな治療法の開発に結びつけて行きたいと考えているという。また、今回報告されたGAD65プロモーターは、遺伝子サイズが約2.5 kbと、やや大きいという特徴がある。このためAAVベクターのパッケージング限界や、他に必要な発現カセット等を考慮すると、最大でも1.3 kb程度までの遺伝子の発現にしか利用できない。「今後、本プロモーターの短鎖化を行うことにより、さらに応用範囲を広げたいと考えている」と、研究グループは述べている。
▼関連リンク
・群馬大学 ニュースリリース




