臨床試験にかかる膨大なコストの軽減につながる鍵となるか
九州工業大学は2月19日、ヒトの全身の代謝を遺伝子レベルからシミュレーションすることができるコンピューターモデル「バーチャルヒト全代謝モデル」の開発に世界で初めて成功したと発表した。この研究は、同大大学院情報工学研究院の倉田博之教授らの研究グループによるもの。研究成果は、「iScience」に掲載されている。
医薬品開発や治療法開発に不可欠な臨床試験は、被験者の安全性や結果の信頼性などを確保するために、膨大な時間と費用を要する。従って、ヒトのコンピューターモデルによって臨床試験を代替することは、医学分野最大のブレークスルーの1つと考えられる。21世紀に登場したゲノム科学やシステム生物学は、遺伝子ネットワークや生体分子(酵素反応)ネットワークが適応や発達を含む多様な生物機能や疾患を生み出すメカニズムを明らかにしている。情報科学やシステム工学が急速に進歩する中、コンピューターを用いてヒトの複雑な生命機能(全身の代謝メカニズム)を遺伝子や分子のレベルから数理モデル化し、すべての生理学的機能をコンピューターでシミュレーション・予測することが期待されている。
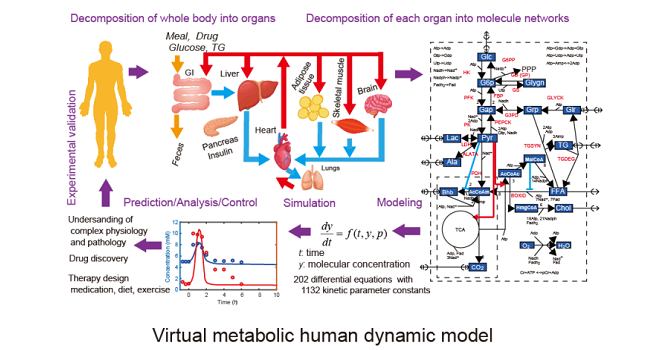
画像はリリースより
1,140の動力学パラメータからなる202の代謝物が時間変化する常微分方程式モデル
今回研究グループは、ヒトの全身の代謝のコンピューターモデルを実現するために、ヒトを構成する生体分子(酵素反応)ネットワーク全体をサブシステムに分解し、それぞれを数理モデル化した後、それらを統合するシステム生物学のモデリング戦略を提案した。具体的には、ヒトの全身の代謝を血液、膵臓、肝臓、骨格筋、脂肪組織、心臓、胃腸、脳の8つの臓器に分解し、各臓器において解糖系、糖新生、β酸化、グリコーゲン蓄積、トリグリセリド合成を含む物質変換とエネルギー変換システムを数理モデル化した後、臓器モデル間を血液中のグルコース、乳酸、アラニン、脂肪酸、トリグリセリドなどを介して結合する1,140の動力学パラメータからなる202の代謝物が時間変化する常微分方程式モデル(バーチャルヒト全代謝モデル)を開発した。
代謝システム中の酵素反応のミカエリス定数パラメータは試験管の実験値を使用。一方、遺伝子発現量に依存して変化する反応速度定数パラメータは、遺伝的アルゴリズムを用いてスーパーコンピューター上で推定した。断片的な生物の測定データから膨大な数のパラメータ値を推定する必要があるため、困難な課題に見えるが、実際は、定性的実験データに基づく制約条件を与えることによって、パラメータ値を推定することを実現した。
開発モデルは、糖尿病の発症メカニズムや新規治療薬を提案
開発したバーチャルヒト全代謝モデルの有用性を検証するため、膵臓が放出するインスリンをレギュレータとし、食後と安静時における各臓器の代謝反応速度や血液中の代謝物濃度変化を確かめた。その結果、正確に再現されたという。これは、開発したモデルが、全身の代謝の最も包括的で高い予測精度をもつコンピューターモデルであることを示している。加えて、脂肪症、膵臓の機能障害、インスリン抵抗性などの個々の障害を組み合わせて、糖尿病を引き起こすメカニズムを明らかにした。また、開発したモデルは、グリセロールキナーゼ阻害剤が2型糖尿病の効果的な薬であることも予測。この阻害剤は肝臓のトリグリセリドを減少させるだけでなく血液中グルコースも減少させており、開発したモデルを用いて、多剤併用療法を合理的に設計することもできたという。
糖尿病など代謝疾患メカニズムを解明し、医薬品の効果予測に貢献
20年前は生物学的複雑性や測定データ不足のため、コンピューターモデルの開発は非現実的といわれていたが、現在、ゲノム科学やシステム生物学の発展によって、ヒト代謝システムの時間変化を予測するコンピューターモデルの開発が可能となった。今後は代謝反応だけでなく、遺伝子発現調節や信号伝達を組み合わせたゲノムスケールのコンピューターモデルの提案が可能になると考えられる。
「生命現象は、それが物理化学プロセスであるという基本にたてば、人工システム(自動車、飛行機、コンピューターなど)と同様に数理モデルの対象だ。生命は、コンピューターシミュレーションのフロンティアであると言える。生物学者や医学者と協力しながら、バーチャルヒト全代謝モデルを革新して、糖尿病などのさまざまな代謝疾患メカニズムを解明し、医薬品の効果を予測することによって、情報科学だけでなく生物医学の発展にも貢献することを目指す」と、研究グループは述べている。
▼関連リンク
・九州工業大学 プレスリリース




