GP2に反応をする自己抗体が炎症性腸疾患の患者で多いことはわかっていたが、その役割は不明だった
千葉大学は2月17日、食物の消化を担う「膵臓」が細菌感染から腸管を守る働きを持つことを初めて明らかにしたと発表した。この研究は、同大大学院医学研究院イノベーション医学研究領域の倉島洋介准教授(東京大学医科学研究所臨床ワクチン学分野特任准教授)と東京大学医科学研究所粘膜免疫学部門の清野宏特任教授(米国カリフォルニア大学サンディエゴ校教授、千葉大学大学院医学研究院特任教授)らの研究グループによるもの。研究成果は、「Nature Communications」に掲載されている。
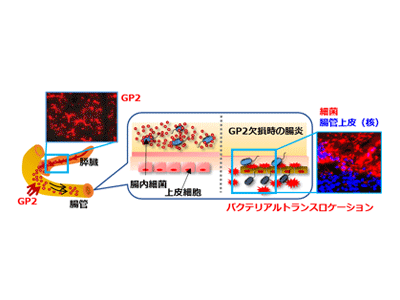
画像はリリースより
膵臓は、食べ物を消化する膵液を十二指腸内へ分泌し、腸管での消化を助ける外分泌機能を持つ。この外分泌機能を担う膵臓の腺房細胞の分泌顆粒には、GP2が多く含まれている。GP2はアミラーゼなどの消化酵素が含まれる顆粒の顆粒膜タンパク質のうち、15~30%を占めるといわれており、大量に分泌され、腸管腔に広く分布している。
これまで、GP2の遺伝子変異が膵臓がんのリスクの上昇につながることや、GP2に反応をする自己抗体が炎症性腸疾患の患者で多く検出されることが報告されていたが、膵臓から分泌されるGP2の役割はほとんどわかっていなかった。
また、腸管の機能低下が多臓器不全を引き起こすメカニズムには、炎症性腸疾患などの消化管疾患や免疫能の低下、全身的な栄養不全、ストレス、細菌の異常増殖により、生きた腸内細菌が腸管内から粘膜組織や腸管のリンパ節、他の臓器へと移行・感染する「バクテリアルトランスロケーション」と呼ばれる現象が関与していると考えられている。この現象に対して生体内が持つ防御機構を調べることや、仕組みを紐解き、それを活用することでバクテリアルトランスロケーションによって悪化する多くの疾患に対する予防法や治療法への応用が可能だと考えられてきた。しかし、バクテリアルトランスロケーションが起こる明確な原因は明らかにされていなかった。
膵臓から大量に分泌されるGP2が腸内細菌の線毛を捉え、組織中への移行を抑制
研究グループは、これまで炎症性腸疾患や食物アレルギーといった免疫疾患の研究をしており、中でも粘膜に覆われた腸管で起こる免疫応答に特に注目し、研究を進めてきた。その過程で腸管内の細胞に発現するさまざまなタンパク質を染色し、GP2を発現する細胞についての分布を調べていたところ、当初の目的だった腸管の細胞ではなく、腸管の内容物(管腔)に強くGP2が検出されることを発見した。GP2は腸管の十二指腸から大腸にかけて管腔内に分布しており、糞便中でも多く検出された。
また、腸管内容物に含まれるGP2と腸内細菌を注意深く観察してみると、GP2が腸内細菌と結合し凝集している様子が示された。GP2は細菌の線毛と呼ばれる上皮細胞への接着に必要な部位に結合しており、全身もしくは膵臓特異的にGP2を欠損させたマウスでは、バクテリアルトランスロケーションが起こりやすく、腸炎が重症化することがわかった。さらに、GP2は恒常的に膵臓から分泌されている一方で、腸管からの炎症シグナル(サイトカイン)を腺房細胞が感知することで、より多くのGP2が作られ、膵液中のGP2レベルが上昇するフィードバック機構が存在することが示された。
これらの結果から、腸管の上部に位置する膵臓の新しい役割として、バクテリアルトランスロケーションや食物などからの細菌感染から体を守る粘膜の第一線のバリアとして働いていると考えられるという。
膵臓と腸が連携するメカニズムが、疾患予防や治療法への応用につながる可能性
今回の発見により、外分泌および内分泌を主要な働きとする器官である膵臓が、腸管粘膜に対する潜在性・病原性細菌の感染防御という新しい役割を担っていることが明らかにされた。膵臓と腸が連携するメカニズムのさらなる解析と活用法の開発は、バクテリアルトランスロケーションによって悪化する多くの疾患に対する予防法や治療法への応用につながると期待される。
「他の臓器から発せられる危険信号を感知し保護するという、2つの臓器「膵-腸」の新たな結びつきが明らかになり、栄養やプロバイオティクス、創薬という観点から、この機能の適正化を促すことで疾患の予防や治療に貢献したいと考えている」と、研究グループは述べている。
▼関連リンク
・千葉大学 ニュース・イベント情報




