脂肪細胞におけるGPRC6Aシグナルの脂肪蓄積制御メカニズムを解析
九州大学は2月10日、脂肪細胞におけるGPRC6Aシグナル不全が脂肪の分解を抑制し、食餌誘発性の肥満とそれに起因する代謝異常を引き起こすことを明らかにしたと発表した。この研究は、同大大学院歯学研究院OBT研究センターの向井悟学術研究員(研究当時、現東亜大学医療学部准教授)、溝上顕子准教授、福岡歯科大学口腔医学研究センターの平田雅人客員教授らの研究グループによるもの。研究成果は、「Journal of Biological Chemistry」に掲載されている。
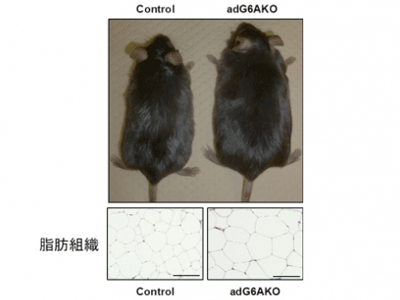
画像はリリースより
GPRC6Aは、骨ホルモンであるオステオカルシン、オルニチンといったアミノ酸、テストステロン、細胞外Ca2+などの多様な分子に応答する。GPRC6Aを持たないマウスは、メタボリックシンドロームが進行したり、骨量が減少したりとさまざまな異常を示すことが既に報告されていたが、その詳細な役割は不明だった。研究グループはこれまでに、特に脂肪細胞のGPRC6Aがオステオカルシンにより活性化し、脂肪細胞を縮小させることを明らかにしている。そこで、脂肪細胞におけるGPRC6Aシグナルが重要ではないかと考え、脂肪特異的にGPRC6Aを持たないマウス(adG6AKO)を作製し、GPRC6Aを介したシグナル経路が脂肪蓄積を制御するメカニズムを解析した。
脂肪特異的にGPRC6Aシグナルを断ったマウスはメタボに
解析の結果、adG6AKOマウスを高栄養食で飼育すると、GPRC6Aを持つマウスと摂食量はほぼ同じであるにも関わらず体重増加が著しいとわかった。また、adG6AKOマウスの脂肪細胞は著しく肥大しており、肝臓への脂肪蓄積も顕著だった。脂肪細胞における脂肪酸取り込み、中性脂肪合成、脂肪分解の各ステップに関わる分子群の発現を比較したところ、adG6AKOマウスの脂肪組織では脂肪を分解する酵素群が著しく減少しており、脂肪分解が抑制されていた。この結果adG6AKOマウスでは肥満、高血糖、耐糖能異常などのメタボリックシンドローム様を呈することがわかった。
さらに、GPRC6Aは多様な分子に応答するが、今回の研究では脂肪分解酵素の発現を上昇させるにはオステオカルシンとオルニチンが最も有効であったことから、脂肪細胞をオステオカルシンやオルニチンで刺激した。すると、脂肪分解酵素群の発現は増加した。これは、adG6AKOマウスの肥満は、オステオカルシンやオルニチンによる恒常的なGPRC6Aシグナルがなくなったことによって脂肪分解酵素が減少し、脂肪分解が抑制されたことに起因することを示すという。以上より、脂肪細胞におけるGPRC6Aシグナルの恒常的な活性化が脂肪の分解を促進し、全身の代謝調節に重要な役割を果たしていることが明らかになった。
研究グループは、「脂肪組織におけるオステオカルシンやオルニチンによる恒常的なGPRC6Aシグナルが肥満を抑制することが今回明らかになった。この成果が肥満治療法開発につながればと思う」と、述べている。
▼関連リンク
・九州大学 研究成果




