自閉症患者で変異率が最も高いCHD8はクロマチンリモデリング因子
九州大学は2月3日、自閉症の原因タンパク質であるCHD8が、造血幹細胞の機能維持に重要な役割を果たすことを明らかにしたと発表した。この研究は、同大生体防御医学研究所の中山敬一主幹教授、仁田暁大学術研究員、金沢大学医薬保健研究域医学系の西山正章教授らの研究グループによるもの。研究成果は、「Cell Reports」に掲載されている。
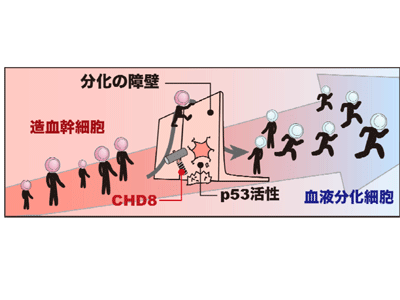
画像はリリースより
自閉症は有病率1%を越える非常に頻度の高い神経発達障害で、胎生期の神経発生の異常により発症する脳の疾患。近年の自閉症患者による遺伝子変異解析により、クロマチンリモデリング因子の1つであるCHD8が最も変異率の高い遺伝子であることが報告されたことで、非常に注目されている。研究グループは世界に先駆けてCHD8遺伝子に変異を持つ「自閉症モデルマウス」の作製に成功し、CHD8変異による自閉症発症メカニズムの解明を行ってきた。
非神経系、特に造血幹細胞でも発現のCHD8、そこにおける役割は?
CHD8は自閉症の原因遺伝子であるため、多くの研究が神経系に特化したものである一方で、CHD8の発現は非神経系でも非常に高く発現している。特に胚性幹細胞や組織幹細胞など未成熟な細胞で高発現していることがわかっていたが、非神経系の組織幹細胞でのCHD8の機能はほとんどブラックボックスとなっていた。
研究グループは今回、非神経系の組織幹細胞におけるCHD8の機能を評価するために、組織幹細胞研究でも多くの知見がある造血幹細胞の機能評価に着手した。造血幹細胞は、機能をもつ血液細胞を産生するまでに分化段階があるため、まず初めに、野生型のマウスの造血幹細胞と造血幹細胞から分化した細胞を各分化段階でCHD8の発現量を比較した。その結果、CHD8は造血幹細胞で最も発現していることが明らかとなった。
CHD8欠損マウスで造血幹細胞の機能消失・異常増加と汎血球減少を確認
次に血液細胞特異的にCHD8を欠損するマウスを作製して解析。その結果、CHD8を欠損した造血幹細胞は異常に増加しており、造血幹細胞から分化した細胞は顕著に減少していることが明らかとなった。さらに、末梢の血液細胞は有意に減少していることから汎血球減少を引き起こしていることが判明した。また、増加した造血幹細胞は機能が消失していた。
続いて、CHD8欠損により造血幹細胞から血液細胞の供給ができない原因を調べるために、RNAシークエンスでCHD8欠損造血幹細胞の遺伝子発現状態を網羅的に評価すると、がん抑制遺伝子のp53の下流遺伝子の発現が顕著に上昇していた。この結果から、定常状態でCHD8がp53活性を抑制していることが考えられるという。
CHD8欠損<p53活性化<造血幹細胞機能に障害
p53は細胞増殖や細胞死に深く関与しているため、CHD8欠損造血幹細胞の細胞周期およびアポトーシスを評価した。その結果、CHD8欠損造血幹細胞は細胞周期が停止しており、さらに、これらの細胞周期が停止した造血幹細胞はアポトーシスを引き起こしていた。したがって、CHD8を欠損した造血幹細胞はp53活性が上昇することで、造血幹細胞からの分化に障害を来し、下流の血液細胞が産生できなくなるのと同時に、自己複製能を消失した後、アポトーシスを引き起こしていることが示唆された。
最後に、CHD8欠損による造血幹細胞の機能の消失がp53の活性によるものなのかを評価するために、血液細胞特異的にCHD8欠損するマウスに、追加でp53遺伝子を欠損するマウスを作製した。解析の結果、CHD8を欠損した造血幹細胞に認められた血液細胞の産生能や自己複製能が、部分的に回復することが明らかとなった。
CHD8変異の自閉症患者治療の重要な知見に
以上の結果より、造血幹細胞においてCHD8を欠損すると、p53が活性化し、造血幹細胞の多分化能や自己複製能に障害を来すことが明らかとなった。これは、CHD8遺伝子に変異を持つ自閉症患者の治療を目指す際の重要な知見となるという。
今回の研究により、CHD8が神経系のみならず、造血幹細胞でも非常に重要な機能を果たすことが示された。自閉症は胎生期の神経発生の異常により発症すると考えられているが、CHD8は出生後でも重要な機能を担っている。今回の研究結果について研究グループは、「今後のCHD8をターゲットとした治療薬を開発する際の一助となることが期待される」と、述べている。
▼関連リンク
・九州大学 研究成果



