COVID-19の初期症状のひとつ、「嗅覚障害」を詳細に研究
東京大学医学部附属病院は2月2日、新型コロナウイルスSARS-CoV-2ウイルス量に関わらず、感染が成立すると感染後数日で広範囲にわたって嗅上皮(鼻の奥にある匂いを感知する部位)が脱落することを明らかにしたと発表した。これは、同大附属病院耳鼻咽喉科・頭頚部外科の山岨達也教授らの研究グループと、テキサス大学医学部ガルベストン校病理学のPaessler Slobodan教授、同・耳鼻咽喉科牧嶋知子准教授らの研究グループとの共同研究によるもの。研究成果は、「ACS Chemical Neuroscience」オンライン版に掲載されている。
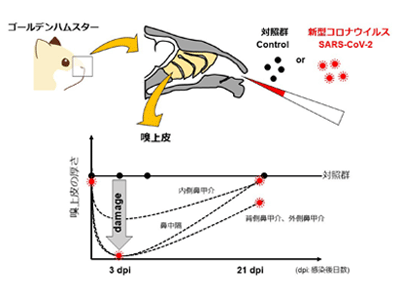
画像はリリースより
嗅上皮には、嗅覚受容体と呼ばれる匂い物質を受け取るタンパク質がある。嗅覚受容体は嗅上皮の重要な細胞要素である、嗅神経細胞に存在している。匂い物質が嗅覚受容体に結合すると、嗅神経細胞を介して脳内に信号が伝わり、匂いを感じるだけでなく記憶や情動などの脳機能にも影響する。外界に接している嗅上皮では、常にプログラムされた細胞死(アポトーシス)と再生を繰り返しながら、それらの機能を維持している。
これまでの研究で、一般的なウイルス感染や薬剤による嗅上皮傷害は一過性であり、高度な嗅上皮傷害の場合は永続的に障害が残存することが知られている。SARS-CoV-2によって引き起こされるCOVID-19の初期症状として嗅覚障害があり、COVID-19の早期診断の指標になり得ると注目されている。パンデミックから約1年が経過し、SARS-CoV-2感染の急性症状だけでなく、慢性症状や合併症の報告が出てきた。これまで報告されてきた症例報告では嗅覚障害は完治するとの報告が多いが、最近の研究結果から急性期を脱した人の18~45%で何らかの嗅覚障害が残存していることが明らかとなった。これらの嗅覚障害が完治するのか、嗅覚障害以外の合併症を引き起こし得るのか、などについて明らかにすることが喫緊の課題となっている。
COVID19モデル動物を確立、嗅上皮の脱落と感染後21日でも一部傷害残存を確認
実験動物として用いられているマウス系統は、ウイルス感染への抵抗性があることが知られており、SARS-CoV-2は野生型マウスに感染しないことが明らかになっている。SARS-CoV-2は細胞の表面に存在する受容体タンパク質(ACE2)を介して感染するため、ACE2遺伝子を改変した動物を用いて研究が行われている。一方で、遺伝子改変モデルマウスではSARS-CoV-2感染後数日で死に至るという点から、臨床症状と相同性の高いCOVID-19モデル動物の確立が求められていた。
研究グループはハムスターを用いてCOVID-19と酷似したモデルを確立。さまざまなウイルス量での感染実験を行った結果、ウイルス量に関わらず感染が成立すると、感染後早期に広範囲にわたって嗅上皮脱落が生じることを明らかにした。また、嗅上皮の大部分は感染後21日で正常厚になったが、一部の嗅上皮では傷害が残っていることも判明した。さらに、SARS-CoV-2感染後の嗅上皮は、部位によって傷害程度や再生速度が異なっていることも明らかになったという。
COVID-19モデル動物は、嗅上皮だけでなく全身臓器の解析が可能
今回の研究成果により、SARS-CoV-2感染における嗅上皮傷害では、「ウイルス暴露量は関係ない」「ウイルス感染後早期に嗅上皮脱落が生じる」「感染後21日でも一部の嗅上皮は再生が不完全」ということが明らかにされた。また、今回作成した動物モデルで発熱などの感染症状はなく、COVID19モデルとして有用と考えられる。一方で、さらなるモデルの妥当性を確認する上で、ヒトでの症状、すなわち嗅覚障害を呈しているかを調べる必要があるという。また、SARS-CoV-2感染後21日で正常厚となった嗅上皮の形態や機能が正常化しているのか、菲薄が残存している部位での傷害が永続的なものか、などを調べる必要もある。
研究グループは「本研究の成果により、COVID-19モデル動物で起こっている変化を嗅上皮だけでなく全身臓器で解析することが可能になった。SARS-CoV-2感染による嗅覚障害の病態解明だけでなく、治療シーズ開発を加速させると期待される」と、述べている。
▼関連リンク
・東京大学医学部附属病院 プレスリリース



