化合物-タンパク質結合強度の網羅的予測は予期せぬ副作用回避につながる
京都大学は1月13日、深層学習技術の一手法であるグラフ畳込みニューラルネットワークを用いることで、医薬品の作用標的として特に重要な127種類のタンパク質に対する親和性を化合物の構造情報から予測できる手法を開発し、さらにこの手法で、抗うつ薬の作用点として知られるセロトニントランスポーターに強く作用する化合物を特定、その化合物がマウスで抗うつ作用を示すことを見出したと発表した。この研究は、同大薬学研究科の金子周司教授、永安一樹助教、酒井幸博士課程学生らの研究グループによるもの。研究成果は、「Scientific Reports」に掲載されている。
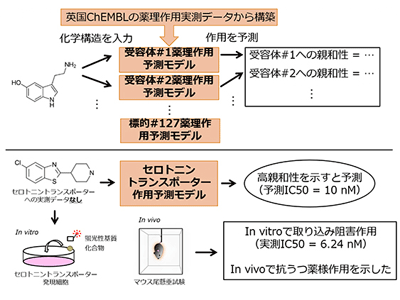
画像はリリースより
現在使われている医薬品の大部分は分子量が小さい化合物だが、この化合物が生体の中のどのようなタンパク質にどの程度の強さで結合するのかを網羅的に実測することは極めて困難だ。一方、化合物が標的としていないタンパク質に予期せず結合してしまうと、医薬品相互作用や副作用の原因ともなる。そのため、任意の化合物がどのようなタンパク質にどの程度の強さで結合するのかを、計算機の上で予測することができれば、新薬開発過程での予期せぬ副作用の発生や、医薬品相互作用を未然に防ぐことができると考えられる。
畳込みニューラルネットワークで127の標的に対する親和性予測モデル構築
そこで、研究グループは、新学術領域「化学コミュニケーションのフロンティア」の支援の下、医薬品-タンパク質結合親和性ビッグデータである英国ChEMBL(ケンブル)に集積されている実測データを用いて、あらゆる化合物のタンパク質結合親和性を予測する手法を開発した。
深層学習技術の一手法であるグラフ畳込みニューラルネットワークを用いることで、医薬品の作用標的として特に重要な127種類のタンパク質に対する親和性を予測できるモデルを構築した。
マウスで抗うつ作用を示す化合物を発見
モデルの妥当性を検証するため、抗うつ薬の作用標的「セロトニントランスポーター」の阻害作用を、実測値がない化合物(CHEMBL1377753)を用いて測定したところ、予測値と極めて近い阻害活性を示すことがわかった。(予測 IC50 = 10nM、実測 IC50 = 6.24nM)。
さらに、この化合物をマウスに投与したところ、運動量には影響することなく、抗うつ作用を引き起こすことがわかった。これらの結果は、構築した予測モデルの高い妥当性を示していると考えられるという。
医薬品作用のデータベースを組み合わせ、ヒトでの作用予測技術開発へ
今回の研究成果により、合成予定の化合物のタンパク質への親和性が計算機上で予測可能となり、目標としていないタンパク質への作用をあらかじめ防ぐことができるようになると考えられる。また、既承認医薬品の適応拡大といったドラッグリポジショニングへの応用も考えられる。一方、ヒトに投与した場合の副作用や薬物間相互作用への直接の応用は難しいことから、今後、医薬品副作用データベースやレセプトデータベースなど、ヒトでの医薬品の作用を集積したデータベースを組み合わせることで、ヒトでの作用予測技術を開発していくことが必要だと考えられる。
研究グループは、「医薬品開発の過程で得られた化合物-タンパク質の結合情報を利用することで、新規の化合物の作用予測ができないか?というアイデアを基に、今回のプロジェクトが立ち上がった。当初の予定を大きく超えて、マウスで抗うつ作用を示す化合物を得ることができた。今後は、ヒトでの治療効果や副作用の予測に向けて研究を深めていきたいと考えている」と、述べている。
▼関連リンク
・京都大学 最新の研究成果を知る



