イレッサによる急性肺障害や間質性肺炎の発症メカニズム解明に向けて
東北大学は1月13日、イレッサ(一般名:ゲフィチニブ)が肺障害を引き起こすメカニズムを解明したと発表した。この研究は、同大大学院薬学研究科の野口拓也准教授、関口雄斗大学院生、松沢厚教授らの研究グループによるもの。研究成果は、英国科学雑誌「Cell Death and Disease」に掲載されている。
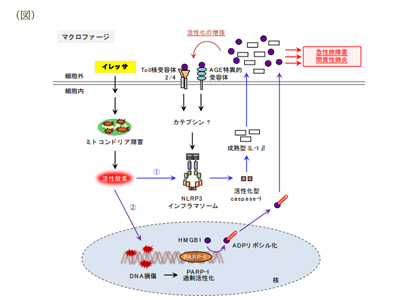
画像はリリースより
イレッサは、がんの増殖に重要な上皮成長因子受容体(EGFR)を選択的に阻害する抗がん剤。2002年7月、世界に先駆けて日本で承認された。現在は約90か国において、EGFR遺伝子変異陽性の手術不能または再発非小細胞肺がんに対して適応されている。
イレッサのような分子標的治療薬は、治療効果と安全性の高さが期待されている。一方で、急性肺障害や間質性肺炎など、イレッサの服用による副作用の報告が出ている。日本では800人以上の服用患者が亡くなったとされている。イレッサによる急性肺障害や間質性肺炎の発症メカニズムは、明らかになっていない。
NLRP3インフラマソーム活性化+PARP-1活性の撹乱で相乗的に炎症を惹起
今回、研究グループは、イレッサが急性肺障害や間質性肺炎などの致死性副作用を引き起こす原因の解明を目的として研究を実施した。
急性肺障害や間質性肺炎は、いずれも炎症性疾患の一種であることから、「イレッサは炎症を惹起する性質を持つ」という仮説を立て、そのメカニズムを解析。その結果、イレッサは免疫応答を担うマクロファージに作用し、2種類の起炎物質インターロイキン-1βとHMGB1の分泌を促進して炎症を惹起していることが判明した。HMGB1にはインターロイキン-1βの分泌を促進する作用があることから、イレッサによるHMGB1の分泌が、インターロイキン-1βの分泌量を増強し、強い炎症の引き金になっている可能性が考えられた。
次に、イレッサがこれら起炎物質の分泌を促す詳細なメカニズムを明らかにした。イレッサは、炎症を誘導するための分子複合体NLRP3インフラマソームを活性化することでインターロイキン-1βの分泌を促す。一方で、イレッサは、DNAの障害などを介した過剰な活性化によって炎症を誘導する働きがある分子PARP-1の活性を撹乱し、それがHMGB1分泌の原因であることも突き止めたという。これらの結果から、イレッサは「NLRP3インフラマソーム活性化」および「PARP-1活性の撹乱」という全く異なる2つのメカニズムを同時に動かし、相乗的に炎症を惹起することが明らかとなった。
インターロイキン-1β分泌遮断マウス、肺炎がほとんど生じず
さらに、インターロイキン-1βの分泌を遮断したマウスは、イレッサによる肺炎がほとんど起きないことが判明。イレッサによる肺障害や間質性肺炎の原因がインターロイキン-1βの過剰分泌であることが示された。
発症予測バイオマーカー開発などに期待
近年、優れた治療効果を示す抗がん剤が数多く開発されている。これらの抗がん剤を安心して服用するためには、抗がん剤による副作用の重篤化を防ぐ必要がある。特に、抗がん剤によって誘導される間質性肺炎は、患者を死に至らしめることもあり、最も警戒すべき致死性の副作用とされている。
今回の研究では、長らく不明であったイレッサによる間質性肺炎の発症メカニズムの一端を解明した。同研究成果は、イレッサによる間質性肺炎の発症を予測するバイオマーカーの開発やその予防・治療法開発につながることが期待されるだけでなく、その他の抗がん剤による間質性肺炎発症機構の解明の一助となることが期待される、と研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース



