TIL培養用のPBMC採取から始め、3月に治療開始予定
日本医療研究開発機構(AMED)は1月5日、「子宮頸がんを対象とした腫瘍浸潤リンパ球輸注療法(TIL療法)」について、厚生労働省へ第3種再生医療等提供計画としての届け出を行い、第2相臨床試験を開始したと発表した。この研究は、慶應義塾大学医学部産婦人科学教室の青木大輔教授、岩田卓専任講師、国際医療福祉大学の河上裕医学部長(同免疫学教室教授、慶應義塾大学医学部先端医科学研究所細胞情報研究部門特任教授を兼任)らの研究グループによるもの。
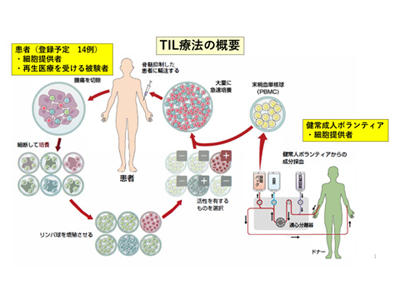
画像はリリースより
なお、同治療では、まずTIL製剤の原料として、健常人ドナーから末梢血単核球(PBMC)を採取する必要があるため、患者への治療開始は3月を予定。TIL療法は、2019年11月に慶應義塾特定認定再生医療等委員会により第3種再生医療等提供計画として適と判定され、2020年12月厚生労働省先進医療会議先進医療として許可された。
最新の全国統計によれば、日本では年間約1万1,000人が子宮頸がんに罹患し、約2,900人が死亡している。子宮頸がんの罹患ピークは40代で、固形がんとしては最も若年者の割合が高い。15~39才の思春期および若年成人の女性では、乳がんに次いで2番目に罹患数・死亡数の多いがんだ。このため、未婚女性や子育て中の母親が罹患する場合も多く、社会的にも大きな問題になっているといえる。
子宮頸がんの初回治療法は、手術または放射線療法。再発した場合は極めて難治性で、進行を遅らせるための姑息的治療として化学療法が主に選択される。子宮頸がんで有効とされる抗がん剤はプラチナ製剤とタキサン製剤に限られ、分子標的薬ではBevacizumabのみが保険適応。他のがんに比べ治療薬の選択肢が極めて少ないのという現状だ。近年注目されている免疫チェックポイント阻害薬は、遺伝子変異が多いマイクロサテライト不安定性(MSI)陽性がんであれば、子宮頸がんでも適応となるが、その割合は数%とされている。
TIL療法実施可能施設、世界でも約10施設のみ
TIL療法は、患者本人のがん組織に含まれる免疫細胞のTILを採取し、体外で大量に培養したものを患者にTILを戻す養子免疫療法の一種。TIL療法は米国を中心に、1980年代より主に進行悪性黒色腫に対して実施され、治療効果が報告されてきた。
2015年、米国のRosenberg博士らが9例の子宮頸がんに対してTIL療法を行い、3例(33%)の患者で腫瘍が縮小し、このうち2例(22%)が完全に腫瘍が消失したと報告。米国では子宮頸がんに対するTIL療法の企業治験も始まり、注目を集めている。
TIL療法の特徴は、著効していったんがんが消滅した場合、その後の再発がなく完治する可能性もあることだ。実際、Rosenberg博士らの治療で腫瘍が消失した2例は、その後5年以上再発していないという。しかし、同治療は、高度なTILの培養技術が必要なため、実施可能な施設は世界でも約10施設にとどまる。
進行子宮頸がん最大14例を対象に、TIL療法を実施
河上教授らは、このTILの培養技術を日本で最初に確立し、すでに2005年に3例の悪性黒色腫患者にTIL療法を実施。この経験を生かし、今回、最大14例の進行子宮頸がんを対象として、TIL療法を実施する。
TIL療法を受ける患者は、2度の入院が必要となる。1度目の入院では、TILを入手するための腫瘍切除術を実施。そして、細胞培養センターで、切除した腫瘍からTILを分離し、培養を開始する。最終的にTILを約100億以上に増殖させ、患者に投与する。なお、このTILの大量培養の過程では、リンパ球を増やすために他人のPBMCが必要となる。今回の試験では患者1人当たり3人のボランティアからPBMC提供を受け、TIL培養に使用するという。
患者は、手術から2~3週間後に2度目の入院。治療前の準備として、投与したTILが体内で増えやすい状態にするために、薬剤投与による骨髄抑制処置を行う。その後で、細胞培養センターから搬送したTILを患者に点滴投与し、さらにリンパ球を増やすIL-2を8時間ごとに最大5回、静脈投与する。患者の骨髄抑制が回復したことを確認し、投与後およそ10日程度で退院となる。投与後4週目と8週目で治療効果を判定するとしている。
なお、この治療は、子宮頸がん患者に対してTIL療法を実施する日本で最初の臨床研究。そのため、研究に参加する患者の安全性を最優先に行う、としている。
▼関連リンク
・日本医療研究開発機構(AMED) プレスリリース



