Smadを介してシグナル伝達を行い、骨形成関連遺伝子発現を誘導するBMP
大阪大学大学院医学系研究科・医学部は12月15日、骨形成タンパク質(BMP)の新たな制御機構を明らかにしたと発表した。この研究は、同大病院の串岡純一医員、同大大学院医学系研究科の海渡貴司講師(整形外科学)らと、愛媛大学大学院医学系研究科の今村健志教授らの研究グループによるもの。研究成果は、「Bone Research」に掲載されている。
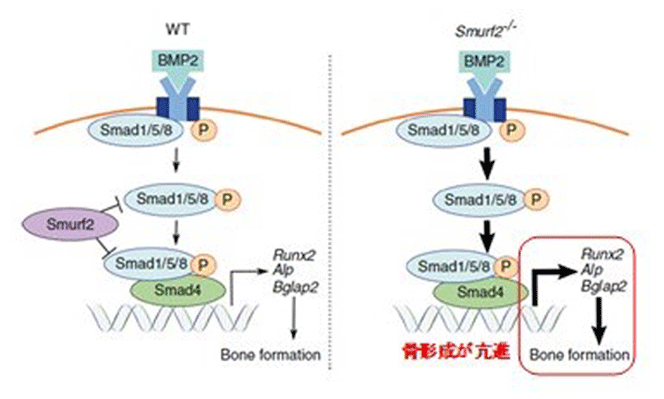
画像はリリースより
骨の石灰化に関わる骨芽細胞の分化を誘導するシグナル伝達経路として、TGF-βを介した経路と骨形成タンパク質(BMP)の経路が知られている。TGF-βおよびBMPは、それぞれの受容体に結合すると細胞内でSmadというタンパク質を介してシグナル伝達を行い、骨形成関連遺伝子発現を誘導する。シグナル伝達が過剰になると、細胞内に過剰発現したタンパク質はユビキチン化により分解を受けて過剰なシグナル伝達が抑制される。
これまでSmadユビキチン化制御因子2(Smurf2)は、SmadのサブタイプであるSmad2/3をユビキチン化することによりTGF-β経路を制御すると考えられていたが、BMPの制御における役割については解明されていなかった。
Smurf2がBMPの細胞内Smad経路を負に制御することにより、BMPによる骨誘導能を負に制御
研究グループは今回、Smurf2欠損状態でBMPを用いて骨形成を誘導することにより、Smurf2のBMPの制御について検討した。Smurf2欠損マウスに骨形成タンパク質(BMP)を含侵したコラーゲンスポンジを背部に移植して異所性骨を誘導すると、Smurf2欠損状態では異所性骨量が大きく、骨形成速度が速くなることを解明した。また、Smurf2欠損状態では骨芽細胞数が増加しており、移植コラーゲンスポンジの内部まで骨形成が認められた。これは、Smurf2がBMPの作用を抑制していることを示すという。
同様に、Smurf2欠損細胞にBMPを添加培養すると骨分化能が亢進した。さらに、Smurf2はSmad1/5をユビキチン化しており、Smurf2欠損細胞にBMPを添加培養するとBMPの細胞内シグナル伝達を司るリン酸化Smad1/5/8発現が上昇していた。反対にSmad1/5/8を阻害すると、BMPを添加培養したSmurf2欠損細胞の骨分化能は低下した。
以上のことから、Smurf2はBMPの細胞内Smad経路を負に制御することにより、BMPによる骨誘導能を負に制御することが明らかになった。
低用量のBMPで安全・効率的に骨形成が制御できる骨再生治療への応用に期待
今回の研究成果により、Smurf2によるBMPの負の制御機構が明らかにされたことで、骨形成タンパク質(BMP)の効果を、より安全・効率的に制御することが期待される。それにより、BMPを臨床使用する際に問題となっている投与箇所の炎症反応や目的外の箇所に骨ができる異所性骨化などの副作用を抑制し、難治性骨折・脊椎固定術・巨大骨欠損を伴う骨腫瘍等へのより安全な骨再生治療への応用も期待される。
「本研究成果により、BMPシグナルを適切に制御することにより、低用量のBMPによる効率的な骨再生治療法の確立につながる可能性が示された」と、研究グループは述べている。




