マスト細胞の低応答化と制御性T細胞の増加がどのように関連しているのか?
千葉大学は12月7日、食物アレルギーの唯一の治療法でありながら、その機序についていまだ不明点が多かった経口免疫療法の治療メカニズムの一端を解明したと発表した。これは、同大大学院医学研究院・倉島洋介准教授、東京大学医科学研究所・清野宏教授、高里良宏医師の研究グループと、慶應大学、順天堂大学、日本大学、カリフォルニア大学を含む多施設との共同研究によるもの。研究成果は、「Mucosal Immunology」オンライン版に掲載されている。
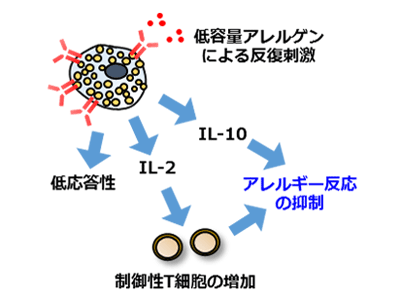
画像はリリースより
食物アレルギーは、白血球の一種であるマスト細胞がアレルゲンを受容し、ヒスタミンなどのアレルギー物質を放出することで発症する疾患。日本で約120万人の患者がいるとされており、かゆみやじんましん、おう吐、下痢のほか、最悪の場合、ショックを起こして死に至るケースもある。
研究グループは今回、食物アレルギーの有望な治療法である経口免疫療法に着目した。しかし、同治療法は研究段階であり、どのような作用機序でアレルギーの根治につながっているのかについての情報は多くない。また、治療中の副反応や成功率の低さも課題となっている。これまで、経口免疫療法を行うことで、ヒスタミンを産生しアレルギーを発症させるマスト細胞の低応答化とアレルギーの抑制細胞である制御性T細胞が増えるという2つの現象は知られていたが、治療の中でマスト細胞の低応答化と制御性T細胞の増加がどのように関連しているのかは不明だった。
経口免疫療法の成功には、マスト細胞自身がアレルギーを抑える細胞へと機能を転換させるメカニズムが重要
研究グループは、独自に食物アレルギーの経口免疫治療モデルマウスを作製し、実験を行った。その結果、経口免疫療法を行いアレルギー症状が軽減された群では、マスト細胞は低応答の状態になるだけでなく、アレルギーを抑制する制御性T細胞を増やすタンパク質(IL-2)や、アレルギー症状を抑えるタンパク質(IL-10)を産生し、アレルギーを起こす悪玉細胞からアレルギー反応を抑える善玉細胞へとその性質が変化していることを発見した。また、食物アレルギーの経口免疫治療の途中にマスト細胞をマウスの体から除去したところ、制御性T細胞が減少すると同時に制御性T細胞のアレルギーを抑える性質も低下していることも明らかになった。
さらに、経口免疫療法を試験管内で模倣したところ、アレルギーの抑制物質を放出するように変化した善玉マスト細胞の作製に成功した。つまり、経口免疫療法によるアレルギー治療の成功には、アレルギーを起こすマスト細胞がアレルギー物質を放出させないように低応答化するだけではなく、マスト細胞自身がアレルギーを抑える細胞へと機能を転換させるメカニズムが重要であることが判明した。
今回の研究成果により、不明点が多かった経口免疫療法を成功させる鍵の一つが明らかとなった。今後は、アレルギーの悪玉細胞を善玉細胞へと効率的に切り替えるスイッチ機構が明らかになれば、それを応用した切り替え促進薬の開発が期待される。「スイッチ機構を制御し悪玉細胞から善玉細胞への切り替えを安定して行えるようにすることで、食物アレルギー治療の精度向上に貢献できると考える」と、研究グループは述べている。
▼関連リンク
・千葉大学 ニュースリリース






