「皮膚線維化」が起こるメカニズムの詳細は、明らかにされていなかった
筑波大学は12月1日、慢性移植片対宿主病では、急性の場合と比べ、表皮を構成する角化細胞において、線維化を誘導するサイトカインの一つであるトランスフォーミング増殖因子β(Transforming growth factor:TGFβ)が強く発現していることを見出したと発表した。この研究は、同大医学医療系の沖山奈緒子講師らの研究グループによるもの。研究成果は、「Journal of Investigative Dermatology」に掲載されている。
画像はリリースより
移植片対宿主病は、血液悪性疾患に対する治療として行われる同種異系骨髄移植の副作用であり、ドナー骨髄細胞が、異なる主要組織適合遺伝子複合体(Major histocompatibility complex:MHC)を持つレシピエント臓器組織を非自己と認識して攻撃することで起こる。
その対象臓器は主に皮膚粘膜、肝臓、腸管で、急性期には皮膚粘膜では時にびらん化する丘疹・紅斑が生じ、表皮に多数のアポトーシスが認められる苔癬反応(Interface dermatitis)という病理組織像を呈する。適切な免疫抑制治療により寛解が継続できる症例も多くあるが、慢性期に移行した、もしくは慢性期になってから発症した症例では、扁平苔癬様と称される、病理学的には苔癬反応を呈する角化性紅斑や、口腔内びらんと瘢痕化、爪甲の破壊と萎縮、斑状または強皮症様びまん性皮膚線維化が混じる症状となり、患者のQOLを著しく低下させる。これらの炎症反応はドナー由来の細胞傷害性CD8T細胞によるものと考えられる。
皮膚線維化は炎症後のリモデリングであると一般に理解されているが、その詳細は不明で特異的な治療法も存在しない。他に苔癬反応を呈する疾患である重症薬疹のStevens-Johnson症候群や、中毒性表皮壊死症、膠原病の皮膚ループスエリテマトーデスでも皮膚線維化が起こり、眼粘膜の線維化では失明の恐れもある。一方、同様に表皮・上皮に生じる炎症性皮膚粘膜疾患であっても、苔癬反応を呈さない接触皮膚炎、アトピー性皮膚炎、乾癬などでは、皮膚線維化は大きな問題にならない。また、II度熱傷では表皮が欠損しても線維化を残さず治癒するが、真皮まで大きく欠損するIII度熱傷では線維化し、瘢痕拘縮(引きつれ)を残す。このように、リモデリングといっても、皮膚線維化を残す場合と残さない場合があり、その機構は明確ではない。
角化細胞がアポトーシスに陥るときに皮膚線維化を起こすことが、リモデリングの本態である可能性
研究ではまず、慢性移植片対宿主病症例の皮膚生検検体では急性移植片対宿主病症例の検体と比べ、表皮角化細胞が、代表的な線維化誘導サイトカインであるTGFβを強く発現していることを見出した。
そこで、皮膚粘膜移植片対宿主病のモデルマウス(OT-I細胞移入ケラチン14プロモーター下卵白アルブミントランスジェニックマウス:OT-I cell-transferred K14-mOVA Tgマウス)を用いて、皮膚線維化が生じる機構を詳細に解析した。すると、このモデルマウスでも、OT-I細胞移入後2週間以内には、びらん化する急性移植片対宿主病様皮膚粘膜疾患を発症するが、移植後28日目にはびまん性皮膚硬化により、強皮症様の慢性移植片対宿主病様皮膚線維化を呈した。その際、皮膚に浸潤するOT-I細胞は、細胞死を誘発するタンパク質分解酵素であるグランザイムBを産生して表皮角化細胞死を誘導するが、同時に、代表的な炎症性サイトカインであるインターフェロン(IFN)γも産生しており、このとき角化細胞はTGFβを強く発現していた。一方、IFNγ欠損OT-I細胞移入時には、レシピエントK14-mOVA Tgマウスは急性移植片対宿主病様皮膚粘膜傷害を起こすものの、その後の慢性移植片対宿主病様皮膚線維化は起こさなかったという。
培養角化細胞を用いた実験では、角化細胞にさまざまな細胞死の形態である、ネクローシス(損傷などによる偶発的な細胞の膨張破裂)、アポトーシス(プログラムされた細胞死)、ネクロプトーシス(制御されたネクローシス)を誘導したところ、アポトーシスとなった角化細胞が最も多くのTGFβを産生した。また、この産生はIFNγ添加によって増強され、アポトーシス阻害薬添加によって抑制された。
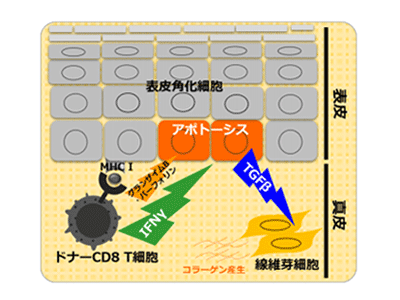
これらのことから、慢性移植片対宿主病においては、皮膚に浸潤してきた病原性CD8T細胞がIFNγを産生しながら、パーフォリン-グランザイム経路を使って角化細胞をアポトーシスに陥らせると、その角化細胞がTGFβを産生し、真皮の線維芽細胞に働きかけて皮膚線維化を誘導していることが示唆された。つまり、角化細胞がアポトーシスに陥るときに、皮膚線維化を引き起こしてしまうことが、この病態における「リモデリング」の本態と考えられたという。
IFNγ標的治療やアポトーシス阻害薬が、線維化制圧のための治療選択肢となることに期待
今回の研究成果により、慢性移植片対宿主病のみならず、皮膚線維化を残すことが問題となる重症薬疹のStevens-Johnson症候群や中毒性表皮壊死症、膠原病の皮膚ループスエリテマトーデスにおいて、IFNγ標的治療やアポトーシス阻害薬が、線維化を制圧するための治療選択肢となり得ることが示唆された。
IFNγは線維芽細胞に添加するとコラーゲン産生を抑制することから、長く「抗線維化サイトカイン」とされており、これを、全身性の線維化疾患である、膠原病の強皮症の治療に使う試みも行われてきたが、成功には至っていない。同研究成果は、その理由が、IFNγが角化細胞を介して線維化誘導をしている経路があるためであることも示している。
アポトーシス阻害薬は、肝硬変治療薬やアルツハイマー病治療薬などで臨床応用に向けて研究が進められており、慢性移植片対宿主病のような角化細胞アポトーシスを基盤とした皮膚線維化疾患に対する臨床応用も期待される。
▼関連リンク
・筑波大学 注目の研究




