長鎖脂肪酸を細胞内で輸送するタンパク質FABP3
東北大学は11月2日、アレルギー性皮膚炎の発症制御において脂肪酸結合タンパク質3型(FABP3)が重要な役割を果たしていることを、モデルマウスの研究において明らかにしたと発表した。この研究は、同大大学院医学系研究科器官解剖学分野の小林周平助教と大和田祐二教授ら、同免疫学分野、および慶應義塾大学医学研究科の研究グループによるもの。研究成果は、欧州アレルギー学会雑誌「Allergy」電子版に掲載されている。
アレルギー病態には、遺伝的・環境的要因が複雑に関与することが知られている。近年、食物からの栄養摂取により免疫細胞の機能が変化し、アレルギー病態に影響を与える可能性が示されているが、そのメカニズムについては未だ不明な点が多く残されている。
FABP3は、水に不溶な長鎖脂肪酸を細胞内で輸送するためのタンパク質。神経細胞や骨格筋など体内の種々の細胞に広く発現しているが、免疫細胞における分子機能、ひいてはアレルギー病態との関与については明らかではなかった。
画像はリリースより
FABP3欠損マウス、アレルギー性皮膚炎を誘導した耳が顕著に腫れる
今回、研究グループは、FABP3がアレルギー性皮膚炎の発症制御に関与することを発見した。
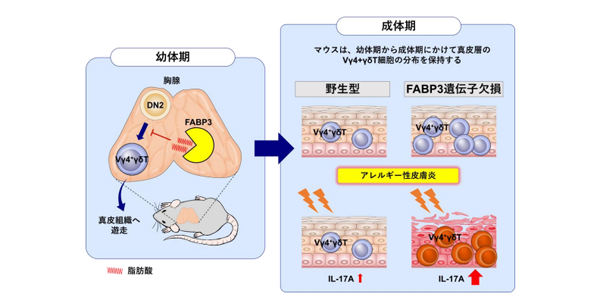
まず、免疫組織である脾臓の免疫細胞においてFABP3の遺伝子の発現を網羅的に調べ、リンパ球(Tリンパ球)の一部の集団でFABP3が発現していることを見出した。そこで、Tリンパ球が原因となる病態モデルとされる薬剤誘導アレルギー性皮膚炎マウスを用いて、リンパ球におけるFABP3の機能とアレルギー病態への関与について検証。その結果、FABP3欠損マウスでは、アレルギー性皮膚炎を誘導した耳が対照(野生型)マウスよりも顕著に腫れており、皮膚炎症の増悪に関与する炎症因子IL-17を産生するTリンパ球(Vγ4+γδTリンパ球)も集積していた。
アレルギー性皮膚炎を誘導する前においても、FABP3欠損マウスでは皮膚組織におけるVγ4+γδTリンパ球細胞の割合が増加していた。そこで、幼体におけるTリンパ球の分化の場である胸腺および成熟後に皮膚に集積するγδT細胞を調べた結果、幼体期のFABP3欠損マウスにおいて、胸腺および皮膚においてVγ4+γδTリンパ球の割合が有意に増加していた。
FABP3、DN2細胞で強く発現
続いて、幼体マウスの胸腺から細胞を分取し、FABP3の発現を調べた結果、一部の細胞(DN2細胞)で強く発現していることが明らかとなった。
さらに、幼体期の野生型およびFABP3欠損マウス由来のDN2細胞のTリンパ球へ分化する能力を試験管内で解析。その結果、FABP3欠損マウス胸腺由来のDN2細胞はVγ4+γδTリンパ球への分化が顕著に亢進していた。
発達期栄養コントロールによるアレルギー疾患発症予防への発展に期待
これらの結果は、FABP3欠損による胎児期または新生児期における脂質の恒常性の破綻が、成人期のアレルギー性疾患の発症に影響を与える皮膚のVγ4+γδTリンパ球の分化を促進することを示している。
胎児期あるいは幼体期に摂取する脂質の量や組成が、成長後のアレルギー性皮膚疾患の発症や増悪に影響する、というDOHaD仮説に基づいた新規の成果。将来的に、発達期の栄養コントロールによるアレルギー疾患発症予防へと発展することが期待される、と研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース




