レナリドミド耐性の多発性骨髄腫でポマリドミドが抗がん作用発揮、その理由は?
東京工業大学は9月23日、多発性骨髄腫の治療薬「ポマリドミド」の抗がん作用に「ARID2」というタンパク質の分解が関わっていると判明したと発表した。これは同大生命理工学院生命理工学系の山本淳一助教と山口雄輝教授、東京医科大学の半田宏特任教授、埼玉医科大学の木崎昌弘教授らの研究グループによるもの。研究成果は、「Nature Chemical Biology」に掲載されている。
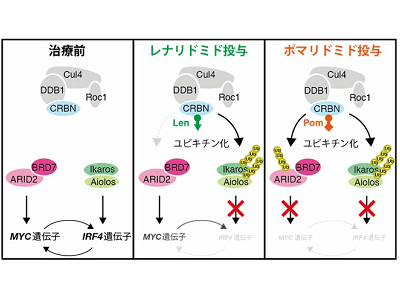
画像はリリースより
多発性骨髄腫は1990年代までは抗がん剤による病勢コントロールが治療の主体であった。2000年以降、新たな治療薬の登場により、その生命予後は大きく改善しているが、多発性骨髄腫は依然として治癒を得ることが難しい血液がんである。
1950年代に鎮静剤として開発された「サリドマイド」は、深刻な催奇形性を有することから世界的な薬害事件を引き起こし、市場から撤退した。しかし、その後の研究からサリドマイドがハンセン病や多発性骨髄腫などの難病に有効であることが明らかとなり、厳格な統制下での投与が再び認可されるに至っている。研究グループは2010年、サリドマイドの分子標的がタンパク質分解を司るユビキチンリガーゼ複合体の構成因子である「セレブロン」というタンパク質であることを明らかにした。その後の研究から、サリドマイド系薬剤がセレブロンに結合すると、その基質特異性が変化し、通常は分解されないタンパク質が分解されるようになることが明らかになってきた。このような特定の薬剤の存在下でのみ分解される標的タンパク質を「ネオ基質」と呼び、サリドマイド系薬剤の多様な薬理作用はさまざまなネオ基質の分解によって引き起こされると考えられている。
サリドマイド誘導体であるレナリドミドやポマリドミドは免疫調節薬とも総称され、多発性骨髄腫の治療薬として用いられている。レナリドミドが多発性骨髄腫の標準治療で用いられているのに対し、ポマリドミドは標準治療に対して無反応だったり再発したりした場合にサルベージ治療に用いられている。レナリドミドやポマリドミドの多発性骨髄腫に対する抗がん作用に関与するネオ基質として、「Ikaros」と「Aiolos」というタンパク質が見つかっているが、これらはレナリドミドでもポマリドミドでも分解され、両者の薬効の違いを説明できない。ポマリドミドがレナリドミド抵抗性の多発性骨髄腫に抗がん作用を示す理由は不明だった。
ARID2が予後不良マーカーとして有用な可能性
今回研究グループは、「ARID2」というタンパク質がポマリドミド特異的なネオ基質であることを明らかにした。ポマリドミドはレナリドミドよりもARID2を分解する活性が遥かに高く、レナリドミド耐性の多発性骨髄腫細胞においてもARID2を分解し、増殖阻害を引き起こした。これらの結果から、ポマリドミドはIkarosとAiolosに加えてARID2も分解に導くことでレナリドミドよりも優れた抗がん作用を発揮していることが示唆された。
また、ARID2が高発現している多発性骨髄腫患者は予後が悪いこと、ARID2が再発・難治多発性骨髄腫患者において高発現していることも判明し、ARID2が予後不良マーカーとして有用であることが示唆された。
ARID2分解<MYC発現低下<多発性骨髄腫死滅
ARID2は、クロマチンリモデリング複合体PBAFを構成するサブユニットの1つである。セレブロンがポマリドミド依存的にARID2を分解する際には、PBAF複合体の別のサブユニットであるBRD7がセレブロンとARID2の間を「橋渡し」していることも当研究グループは突き止めた。また、PBAF複合体が多発性骨髄腫の増殖に必須な「アキレス腱」として知られているMYC遺伝子の発現に重要であり、ARID2が分解されるとMYC遺伝子の発現が低下して、多発性骨髄腫が死滅することも明らかにした。以上の結果から、ARID2はレナリドミド耐性を示す再発・難治多発性骨髄腫の診断や治療において有望な標的であることが判明した。
多発性骨髄腫治療の有望な標的としてARID2が同定され、今後はARID2を標的とした、より効果の高い薬剤の開発が望まれる。「最近の別の研究から、ARID2を含むPBAF複合体が、がん免疫療法に対する耐性に関与することもわかってきている。PBAFを標的とした抗がん剤は多発性骨髄腫だけでなく、さまざまな種類のがん治療に役立つことが期待される」と、研究グループは述べている。
▼関連リンク
・東京工業大学 ニュース






