スプライス変異型の嚢胞性線維症には対症療法しかない
京都大学は9月9日、嚢胞性線維症のスプライス変異でもっとも頻度が高いタイプについて分子病態メカニズムを解析し、リン酸化酵素CLK(CDC-like kinase)を阻害する低分子化合物「CaNDY」を新しい治療薬の候補として同定したと発表した。この研究は、同大大学院医学研究科の萩原正敏教授、網代将彦特定助教、柴田済子博士課程学生の研究グループによるもの。研究成果は、「Cell Chemical Biology」のオンライン版に掲載されている。
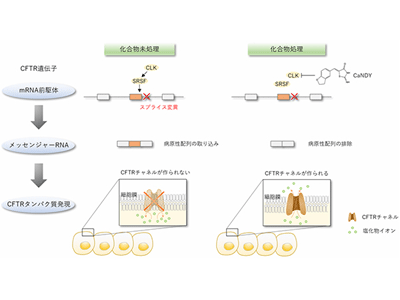
画像はリリースより
嚢胞性線維症はCFTR(cystic fibrosis transmembrane conductance regulator)遺伝子の変異によって引き起こされる難治疾患であり、指定難病となっている。全世界での罹患者は7万人を超え、特に欧州圏では出生約3,000人に1人と高頻度だ。CFTRは細胞膜で塩化物イオンチャネルとして機能するが、遺伝子の変異によってその機能が障害されることで、患者体内では細胞分泌物の組成を正常に調節することが出来なくなる。その結果、気管支、消化管、膵臓などで分泌液粘性が高くなり、細菌などの排除が妨げられることによる感染症リスクの上昇や、炎症等による組織機能の低下が生じる。
これまで嚢胞性線維症の治療法は、分泌物の除去や消化補助剤等の対症療法による治療法しかなく、根本的な原因であるCFTRの機能低下に対する治療方法はなかった。また、有効な遺伝子治療も嚢胞性線維症に対しては確立していない。CFTRの機能を補助する薬剤が近年上市されたが有効性は一部の病型に限られる。特に、V型に分類されるスプライシング変異には有効な治療法がないことが問題になっている。
遺伝子発現の過程でゲノムDNAから転写されたmRNA前駆体は、RNAスプライシングによりエクソンとエクソンがつなぎ合わされ、イントロン配列が除去されるが、スプライシング変異はこの過程に異常を生じさせることで病原性を示す。嚢胞性線維症のスプライシング変異で最も頻度の高い変異はc.3849+10kb C>Tと呼ばれる変異型で、全症例のうち2%未満で生じている。この変異が存在すると第22番イントロンの配列中に新しいエクソンが生じるが、そのエクソン配列が取り込まれることでメッセンジャーRNAの途中で終止コドンが発生しCFTR遺伝子の発現が阻害されることで病原性を呈す。今回、研究グループは、このスプライス変異をモデルとして病原性メカニズムと治療標的の解析を行った。
スプライシングを正す「CaNDY」を同定、投与でCFTRの機能が回復
今回、遺伝子変異周辺の配列情報をもとに関連制御因子の解析を行ったところ、スプライシング制御に関わるRNA結合タンパク質のSRSF(serine/arginine-rich splicing factor)ファミリーが周辺領域に直接結合することがわかった。また、機能喪失実験等の分子生物学的アプローチから、このSRSFファミリーの結合がスプライシング異常に必須であることが判明。さらに、リン酸化反応によりSRSFファミリー分子を活性化させることが知られるCLKを、低分子阻害剤TG003で阻害することにより、CFTR遺伝子のスプライス異常に働くSRSFの機能を抑えスプライシングが正常化されることがわかった。そこで、TG003の類縁化合物700種あまりに対して、研究グループがこれまでに開発した蛍光色素によるリポーターベクターを用いた化合物スクリーニングを実施。その結果、スプライシング正常化の効果が特に高い治療薬の候補として「CaNDY」が選定された。CLKファミリーに対する酵素阻害活性を調べたところ、CaNDYはTG003よりもCLKファミリー全般に高い阻害活性を示し、特にCLK3に対する阻害活性が顕著に向上していた。さらに、CaNDYの投与処理をおこなうと、スプライス変異型のCFTRの機能が正常値付近に回復することがわかった。
今回の研究から、従来対症療法しか無かったスプライス変異型の嚢胞性線維症に対して、病因であるCFTRの機能不全を回復させる新しい治療薬CaNDYが同定された。同様なメカニズムによるスプライス変異は、嚢胞性線維症に限らずさまざまな遺伝性疾患においても報告されている。そのため、CaNDYはそれら疾患においても同様に治療可能性を示すことが期待される。遺伝病発症の分子メカニズムの共通性に着目した疾患横断的な治療法探索は従来の創薬概念を大きく変える可能性がある。一方で、今回の病態モデルにおける治療効果を臨床応用に向けて展開するためには、CaNDYの非臨床物性を最適化するプロセスが必要になる。研究グループは、今後、薬物動態の改善及び安全性の検討を進めていくとしている。
▼関連リンク
・京都大学 研究成果






