生体防御遺伝子を活性化し、ストレスに保護的に働く転写因子Nrf2は宇宙ストレスにも有効か?
東北大学は9月9日、宇宙長期滞在マウスの研究から、宇宙ストレスはさまざまな加齢変化を引き起こし、この加齢変化加速の食い止めにNrf2活性化が重要であることを明らかにしたと発表した。この研究は、同大大学院医学系研究科の鈴木隆史講師(医化学分野)、山本雅之教授(医化学分野、東北大学東北メディカル・メガバンク機構長)および宇宙航空研究開発機構(JAXA)の芝大技術領域主幹らの研究グループによるもの。研究成果は、「Communications Biology」のオンライン版に掲載されている。
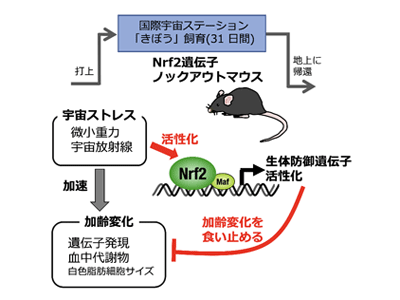
画像はリリースより
同成果は東北大学東北メディカル・メガバンク機構(ToMMo)とJAXAとの「健康長寿社会実現への貢献を目指した「きぼう」利用に係る連携協定(2019年2月8日)」で得られた初の科学成果となる。
人類が宇宙進出を果たすためには、宇宙放射線や微小重力環境などの宇宙環境ストレスによる健康リスクを克服することが必要だ。転写因子Nrf2は、一群の生体防御遺伝子を活性化し、地上におけるさまざまなストレスに対して保護的に働くことが知られている。
研究グループは、この転写因子Nrf2の活性化が宇宙ストレスの防御にも有効ではないかと考え、それを検討・実証する目的で研究を行った。
宇宙ストレスは、さまざまな加齢変化を早回しで引き起こす
2018年4月、野生型およびNrf2遺伝子ノックアウトマウスの雄それぞれ6匹、合計12匹をケネディ宇宙センターから打ち上げ、ISS・「きぼう」で飼育した。約30日間の軌道上滞在を終え、12匹全てが生存して帰還。遺伝子ノックアウトマウスの宇宙滞在後の生存帰還は世界初だという。帰還したマウスの詳細な解析を行った結果、宇宙滞在によってさまざまな臓器でNrf2が活性化していることが判明。また、宇宙滞在マウスでは、各臓器における遺伝子発現や、血中代謝物の変化が確認され、その一部はToMMoが有するコホートデータで観察されているヒトの加齢性変化と同じ変化であることがわかった。さらに、加齢変化でも見られる白色脂肪細胞サイズの肥大化が、宇宙滞在マウスで観察されたという。
宇宙に滞在すると筋肉量の低下など加齢に似た現象が起きることは知られていたが、遺伝子発現や血中代謝物の加齢変化が確認されたのは初めてとなる。これらの宇宙滞在による加齢変化がNrf2遺伝子ノックアウトマウスにおいて加速していることがわかった。このことから、宇宙ストレスはさまざまな加齢変化を早回しで引き起こすこと、そしてNrf2は、その加齢変化に対抗して食い止める役割があることが明らかになった。
Nrf2活性化剤が宇宙滞在時のみならず、高齢者の健康を守る薬の研究に発展する可能性
今回の研究では、世界で初めて遺伝子ノックアウトマウスの宇宙滞在生存帰還実験に成功した。同研究成果は、今後の病態モデルマウスを用いた宇宙実験のロールモデルになると期待される。
また、これまでにNrf2発現量の低いヒト遺伝子多型が知られており、同研究成果は、この多型を持つ人が宇宙滞在における健康リスクが高いことを示している。月や火星への長期滞在を考えると、ヒトNrf2遺伝子多型を調べることで、健康リスクの高い個人を事前に予想することが可能になると期待される。
さらに、地球上では何年もかかるような加齢の実証実験を宇宙で短期間に再現できることも明らかになった。今後、さまざまな実験への応用が期待される。加えて同研究成果はNrf2を活性化する薬剤が宇宙滞在時の健康リスクを克服するために有効であることを示している。これまでにNrf2活性化剤は、糖尿病やアルツハイマー病など、加齢性疾患の予防や治療に有効であることが知られており、多くの製薬企業によりNrf2誘導剤の開発が進んでいる。研究グループは、「今後、Nrf2活性化剤は宇宙滞在時のみならず、地上における高齢者の健康を守る薬の研究に発展することが期待される」と、述べている。
▼関連リンク
・東北大学 プレスリリース




