BRCA1の中心体への局在制御に寄与する「RACK1」の働きを詳しく解析
東北大学は9月8日、遺伝性乳がん・卵巣がん症候群(HBOC)の原因になるBRCA1の結合分子RACK1の中心体複製における新たな役割を明らかにしたと発表した。これは、同大加齢医学研究所腫瘍生物学分野の千葉奈津子教授、吉野優樹助教、小林輝大医学系研究科大学院生(現・杉山医院)らの研究グループによるもの。研究成果は、「Journal of Cell Science」にオンライン掲載されている。
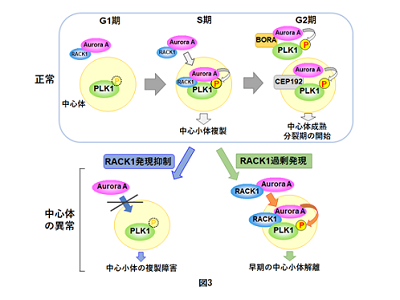
画像はリリースより
BRCA1は、その生殖細胞系列変異によってHBOCを引き起こす。BRCA1はBARD1とヘテロ二量体を形成し、DNA修復、中心体制御に関与する。中心体は、微小管形成中心として機能し、分裂期には紡錘体極を形成し、娘細胞への均等な染色体分配を担う重要な細胞内小器官で、その機能の破綻が発がんの原因になると考えられている。研究グループはこれまでに、BRCA1と結合する新たな分子としてRACK1(Receptor for activated C kinase 1)を同定し、RACK1がBRCA1の中心体への局在の制御に寄与することを報告している。
RACK1はPLK1とAurora Aとの相互作用の「足場」
今回、研究グループは、BRCA1と結合するRACK1が、Aurora Aとpolo-like kinase 1(PLK1)との相互作用の「足場」として働き、S期にPLK1を活性化することで、細胞分裂時の染色体分配に働く中心体の複製に寄与することを明らかにした。Aurora AとPLK1は共に分裂期キナーゼと呼ばれ、細胞分裂の進行に重要な役割を果たすタンパク質として知られている。これらの分子間の結合を助ける足場タンパク質として、BoraやCEP192が知られているが、いずれも細胞周期の主にG2期からM期に働くとされる。S期にPLK1を阻害すると、RACK1を発現抑制した時と同様に、中心小体の複製が抑制されたことから、RACK1で維持されるS期のPLK1の活性が、中心小体の複製に必要であることが示唆された。
RACK1変異は足場としての機能異常をきたし、発がんに関与する可能性
また、がんで高発現が報告されているRACK1の変異の中に、RACK1の足場としての活性に異常をきたす変異が見つかり、これらの変異を有するRACK1は正常の中心体制御活性を失っていることも明らかになった。研究グループは、乳がん細胞でRACK1を過剰発現すると中心体が過剰複製することも報告してきたが、今回RACK1の過剰発現が中心体のPLK1を活性化することもわかった。
今回の研究成果から、RACK1のAurora A/PLK1相互作用の足場としての活性の異常が発がんに寄与する可能性が示された。「Aurora A/PLK1シグナル伝達経路が、がんの治療標的として有望であることが示唆され、新しいがんの治療法開発にも貢献することが期待される」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース



