放射線照射後の「細胞内小胞輸送」に着目して抵抗性のメカニズムを解析
北海道大学は9月2日、神経膠芽腫の放射線治療抵抗性に関与する新たな分子メカニズムを明らかにしたと発表した。この研究は、同大大学院医学研究院の小野寺康仁講師、南ジンミン講師(同大学院医理工学院分子・細胞動態計測分野担当)らの研究グループが、同大学院医学研究院の白土博樹教授(センター長)および清水伸一教授(副センター長)が総括する医理工学グローバルセンターにおいて、米国スタンフォード大学のQuynh-Thu Le教授、Amato Giaccia教授との共同研究として行ったもの。研究成果は、「Neuro-Oncology Advances」にオンライン掲載されている。
画像はリリースより
神経膠芽腫は悪性度が非常に高く、標準治療として放射線療法が用いられているが、いまだに患者の予後が良くない。放射線と抗がん剤の標準治療後、数年以内に再発する場合が多いが、膠芽腫の放射線に対する抵抗性が高いことも、治療の経過がよくない原因の一つとして考えられている。現在の標準治療における放射線は、脳の耐容可能な限度に近い線量が用いられているため、使用総線量を増やさずに放射線治療の効率を上げるための基礎生物学的理解とアプローチが必要とされる。
これまでの研究により、がん細胞から分泌される分泌因子はがん細胞自身または周辺細胞に影響を与えることによって、放射線治療抵抗性において重要な役割を果たしていることがわかってきているが、詳細なメカニズムは明らかにされていなかった。今回、研究グループは、放射線照射後のがん細胞において、細胞内小胞輸送を制御する分子と小胞輸送により分泌される分泌物の変化に着目し、膠芽腫の放射線治療抵抗性に関わるメカニズムを解析した。
放射線照射<Rab27b<エピレギュリン<パラクライン効果<抵抗性
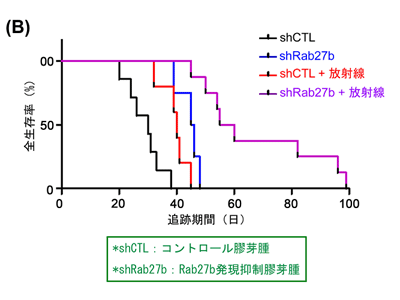
まず、膠芽腫の細胞株を用いて、放射線照射によるRabファミリー低分子量Gタンパク質の遺伝子発現変動をマイクロアレイによって解析したところ、Rab27bの遺伝子発現量が顕著に亢進していた。タンパク質レベルにおいても、非照射細胞に比べて、放射線を照射した細胞でRab27bの発現亢進が確認された。Rab27bの発現を抑制することによって、放射線照射後の細胞死が増加し、細胞増殖が抑制されたことから、放射線による治療の効果を高めることがわかった。さらに、マウス脳への膠芽腫細胞の移植実験において、Rab27bの抑制と放射線照射を組み合わせることにより、脳腫瘍の成長が抑制されマウスの生存期間が延長した。
性質が異なる複数の脳腫瘍細胞株を用いた解析では、悪性度が比較的低い脳腫瘍細胞株に比べて、悪性度の高い膠芽腫細胞株においてRab27bのタンパク質発現が高いことがわかった。これらの細胞では細胞増殖因子であるエピレギュリンの発現も共に亢進しており、これらのタンパク質の発現量が放射線治療抵抗性と相関することが示唆された。また、膠芽腫患者の遺伝子発現プロファイルを解析した結果、Rab27b-エピレギュリンの遺伝子発現の亢進は、膠芽腫患者の予後不良との相関が認められた。
さらに、2種類の異なる脳腫瘍細胞株を用いた共培養実験系により、放射線照射後に膠芽腫から分泌されるエピレギュリンが周辺細胞の増殖に与える影響を解析。その結果、膠芽腫細胞がRab27bを介して分泌するエピレギュリンは、悪性度が低い脳腫瘍細胞株の増殖を促進することがわかった。以上から、膠芽腫への放射線照射後、Rab27bがエピレギュリンの発現および分泌を制御することでパラクライン効果をもたらし、放射線に対する抵抗性を強化することが明らかとなった。
研究グループは、「今後、Rab27b-エピレギュリン経路は、膠芽腫の放射線治療後の腫瘍の増殖を抑え、治療効果を向上させるための新たな標的となる可能性が期待できる」と、述べている。
▼関連リンク
・北海道大学 プレスリリース






