多発性硬化症に代表される脱髄性疾患の多くは原因不明
東北大学は5月19日、脱髄性疾患のうち、髄鞘に存在するタンパク質(ミエリンオリゴデンドロサイト糖タンパク質)に対する自己抗体が原因で血管周囲の神経繊維の脱髄が生じる一群の疾患が、急性散在性脳脊髄炎と似た特徴を持つことを初めて報告したと発表した。この研究は、同大大学院医学系研究科の高井良樹助教、三須建郎講師、青木正志教授を中心とする研究グループによるもの。研究成果は、「Brain」の電子版に掲載されている。
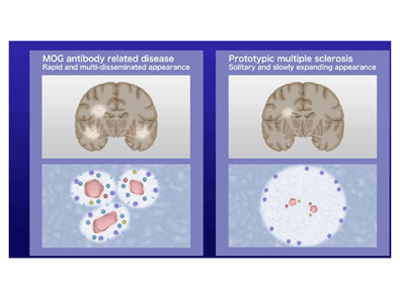
画像はリリースより
多発性硬化症に代表される脱髄性疾患は、異なる自己抗体や免疫細胞応答が複雑に絡み合ったさまざまな病態を有する疾患の集まりであると考えられており、実際に視神経脊髄炎は多発性硬化症から独立した疾患概念となっている。近年、脱髄性疾患の中に、髄鞘タンパク質であるミエリンオリゴデンドロサイト糖タンパク質に対する抗体(抗MOG抗体)が原因となって引き起こされるものがあることが知られるようになり、急性に多発する脳病変、広範囲の脳脊髄の病変や両眼の視神経炎など、多発性硬化症とも異なる特徴を持つことが明らかになってきたが、なぜそのような病変が起こるのかは不明だった。
抗MOG抗体陽性の患者に、急性散在性脳脊髄炎と同様の免疫病理学的特徴
今回、研究グループは、多施設共同研究として、血液中の抗MOG抗体反応が陽性だった患者からの脳組織の標本を11例集め、その臨床病理学的な特徴を調べた。その結果、抗MOG抗体関連疾患における病理組織においては、血管の周囲にリンパ球(CD4陽性細胞やB細胞)やマクロファージといった炎症細胞が浸潤し、血管周囲の神経線維に限局して脱髄が起こる特徴を持つことが判明した。これらの特徴は、急性散在性脳脊髄炎における脱髄の仕組みとして知られてきた特徴と一致すると考えられた。
さらに、血管周囲の脱髄病変を詳しく調べた結果、髄鞘の表面に存在するMOGが選択的に脱落する病変が認められることが明らかとなった。一方、主に髄鞘の内側に存在するミエリン塩基性タンパク質やミエリン随伴性糖タンパク質などは脱髄の病変部位でも比較的保たれており、髄鞘表面のMOGに対する自己免疫応答が起こっていることが示唆された。
MOG抗体関連疾患の特徴は、多発性硬化症や視神経脊髄炎とは異なる
また、MOG抗体関連疾患の特徴と考えられる血管周囲の神経線維の脱髄は、病状が進むと血管周囲の脱髄病変が互いに癒合して、より広範囲な病変となることが明らかになった。その病変の形成過程は急性散在性脳脊髄炎の特徴とよく似ており、全体的に血管周囲に生じた炎症と血管周囲の病巣が互いに癒合して広範囲の病変を形成することが示され、多発性硬化症とは異なる機序で病変が拡大する特徴があることがわかった。
今回の研究によって、抗MOG抗体による脱髄の仕組みが解明され、多発性硬化症や視神経脊髄炎とも異なる特徴を持つ疾患であることが明らかとなった。抗MOG抗体関連疾患は、従来の脱髄性疾患とは適切な治療法も全く異なる疾患であることが示された。研究グループは、「今回の発見により、抗MOG抗体関連疾患の病態の解明や治療法の開発がさらに進むとともに、これまで未解明であった脱髄性疾患の多様性の理解が一層進むことが期待される」と、述べている。
▼関連リンク
・東北大学 プレスリリース



