絶対的なドナー不足で切望される多能性幹細胞による肺臓器の作製
新潟大学は5月13日、胚盤胞補完法を用いて肺臓器を欠損するFgf10ノックアウトマウスの生体内において、マウスES細胞に由来する肺臓器の作出に成功したと発表した。この研究は、同大大学院医歯学総合研究科の北原哲彦大学院生、冉慶松大学院生、周啓亮助教、西條康夫教授らの研究グループが、同大学脳研究所および徳島大学と共同で行ったもの。研究成果は、科学雑誌「Cell Reports」に掲載されている。
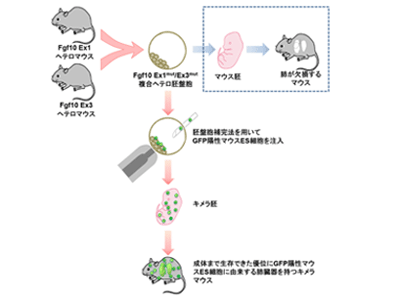
画像はリリースより
多能性幹細胞を用いて肺臓器を作製できれば、これらの問題克服が可能となる。これまでに、多能性幹細胞から2次元プロセスでの肺胞上皮細胞や、気道上皮細胞への分化誘導法や、3次元プロセスでの肺オルガノイドの作製方法、そしてバイオリアクター装置を用いた脱細胞化スキャフォールドによる肺臓器再生などの多能性幹細胞によるin vitro肺再生研究が報告されている。しかし、肺は複雑な3次元構造を持ち、かつ多数の細胞種からなる複雑な臓器であり、in vitroでの移植に耐え得る肺臓器の再構築はきわめて難しいと考えられている。東京大学の中内啓光特任教授らの研究グループは、胚盤胞補完法を用いて、膵臓を欠損させたマウス/ラットの生体内において異種の多能性幹細胞に由来する膵臓を作ることに成功。同様に、腎臓の作製にも成功した。また、同研究とほぼ同じタイミングで、肺形成に必須のFgfr2遺伝子およびβ-Catenin遺伝子のそれぞれで条件付きノックアウトマウスを作製し、胚盤胞補完法により肺の作製に成功したことを報告している。
Fgf10Ex1mut/Ex3mutマウスがES細胞の補完で異常なく生体に発育、肺の大部分がGFP陽性ES細胞由来であることを確認
研究グループは今回、肺臓器そのものの創出を目指し、肺発生に非常に重要なFgf10と、その主な受容体であるFgfr2シグナルに注目し、肺上皮のみならず間葉系の発生にも必須なFgf10遺伝子をノックアウトし、胚盤胞補完法を用いてマウス生体内でES細胞由来肺臓器の創出ができるのではないかと仮説を立てた。
肺や四肢が欠損となるFgf10ノックアウトマウスは出生後に生存できないため、CRISPRA/Cas9システムにてエクソン1(EX1)とエクソン3(EX3)ヘテロマウスをそれぞれ作製し系統維持した。Fgf10 Ex1ヘテロマウスとFgf10 Ex3ヘテロマウスを掛け合わせることで得られた胚盤胞において緑色蛍光タンパクであるGFPを発現するマウスES細胞(Fgf10ワイルド)をマイクロインジェクションした後に、偽妊娠マウス子宮に着床させ、キメラ産仔を得た。キメラ産仔および成体まで飼育されたキメラマウスのゲノム解析、組織学的および機能学的な解析を行い、マウス生体内にES細胞由来の肺臓器が創出されたかどうかを解析した。
Fgf10ホモ欠損胚を使う場合には、ゲノム解析の過程で野生型ES細胞の混入によりFgf10がホモ欠失であることの証明に困難を生じるため、今回の研究ではまず、Fgf10Ex1mut/Ex3mut複合ヘテロマウスを開発し、ホモ欠損と同様に肺及び四肢が欠損することを証明し、簡便かつ高効率なゲノムタイピングすることに成功した。このFgf10Ex1mut/Ex3mut複合ヘテロマウス胚盤胞にGFP陽性マウスES細胞を胚操作のマイクロインジェクションで移入を行い、本来では出産後に生存できないFgf10Ex1mut/Ex3mutマウスがES細胞に補完され、成体まで異常なく発育・成熟した。キメラ産仔および成体キメラマウスを解析したところ、肺の実質部分(肺胞上皮細胞)が優位にGFP陽性ES細胞由来であることを確認した。また、肺臓器の間質部分(血管内皮細胞、血管平滑筋細胞、傍気管平滑筋細胞、結合組織)においても、大部分がGFP陽性ES細胞由来であることを確認した。
肺疾患モデル動物の開発、大型動物における肺臓器創出技術の確立に期待
現行のFgf10Ex1mut/Ex3mut複合ヘテロマウスにおける胚盤胞補完法による肺臓器の創出はキメラ率とキメラリズムがまだ低いため、今後はさらなる胚盤胞補完法の改良が必要と考えられる。研究グループは、「Fgf10以外に肺発生に重要な遺伝子など複数の遺伝子を改変することで、より胚盤胞補完法による肺臓器再生に適切なノックアウトマウスの作製を検討する。さらにその方法を発展させ、異種間キメラでの検討や、肺疾患モデル動物の開発、大型動物における肺臓器創出技術の確立への展開が期待される」と、述べている。
▼関連リンク
・新潟大学 研究成果



