ウイルスのRNAポリメラーゼを選択的に阻害することでウイルス増殖を防ぐ
富士フイルム株式会社は4月9日、抗インフルエンザウイルス薬「アビガン(R)錠」(一般名:ファビピラビル)について、新型コロナウイルス感染症(COVID-19)患者を対象の臨床第2相試験を米国で開始したと発表した。
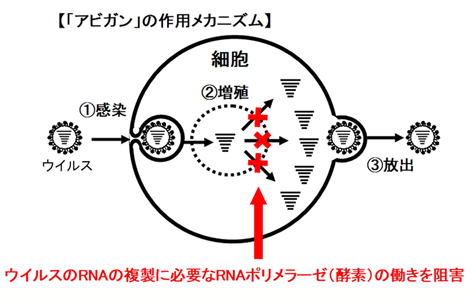
画像はリリースより
アビガンは、同社子会社である富士フイルム富山化学株式会社が開発し、日本において、他の抗インフルエンザウイルス薬が無効または効果不十分な新型または再興型インフルエンザウイルス感染症が発生し、同剤を当該インフルエンザウイルスへの対策に使用すると国が判断した場合に、患者への投与が検討される医薬品として、2014年3月に承認を取得している。同剤は、ウイルスのRNAポリメラーゼを選択的に阻害することでウイルス増殖を防ぐというメカニズムを有している。このようなメカニズムの特徴から、インフルエンザウイルスと同種のRNAウイルスである新型コロナウイルスに対しても効果が期待され、臨床応用への検討が進んでいる。
国内では2020年3月末に臨床試験開始、今回は米国で
国内においては、すでに2020年3月末に富士フイルム富山化学株式会社によって、アビガンのCOVID-19患者を対象とした臨床試験が開始している。今回、同社は、COVID-19の世界的な感染拡大が続き、ますます高まる治療法の開発ニーズに対応するために、米国でも臨床試験を開始。同試験は、数十例のCOVID-19患者を対象とした臨床第2相試験で、アビガン投与時の治療効果と安全性を確認することを目的としている。なお、ブリガム・アンド・ウイメンズ病院やマサチューセッツ総合病院、マサチューセッツ州立大学メディカルスクールの3施設での実施を予定している。
同社は、患者の救済を使命に、早期の治療法確立を図るとともに、国内外のパートナーとの連携によるアビガン増産体制の整備を進めることで、1日も早い、COVID-19の感染拡大の抑止や流行の終息に貢献していく、と述べている。
▼関連リンク
・富士フイルム株式会社 お知らせ




