体節形成を制御する「分節時計」
京都大学は4月2日、ヒト人工多能性幹細胞(iPS)細胞を段階的に誘導する手法を開発し、脊椎の発生を試験管内(in vitro)で再現するモデルを確立したことを発表した。この研究は、同大高等研究院ヒト生物学高等研究拠点(ASHBi)アレヴ・ジャンタシュ准教授(研究当時は京都大学 iPS細胞研究所助教)らの研究グループが、理化学研究所生命機能科学研究センターの戎家美紀ユニットリーダー(現 EMBL Barcelonaグループリーダー)の研究グループ、京大iPS細胞研究所(CiRA)、理化学研究所生命医科学研究センター、名城病院の研究者と共同で行ったもの。研究成果は、「Nature」オンライン版に掲載されている。
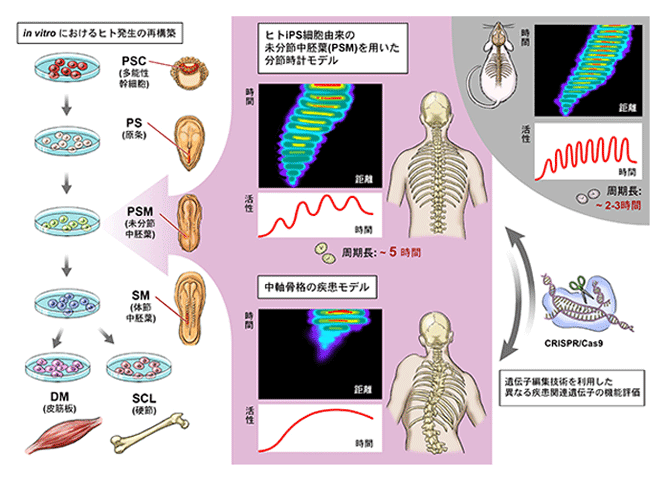
画像はリリースより
体節とは、将来椎骨・肋骨・骨格筋・皮膚などに分化する細胞群。一定時間ごとに、未分節中胚葉(PSM)と呼ばれる分化していない細胞がくびれて切れることにより形成される。この体節形成は胚発生(多細胞生物が受精卵から成体になるまでの過程)における主要な発生プロセスであり、マウス、ニワトリ、ゼブラフィッシュ等のモデル生物で研究されてきた。現在ではモデル動物において、遺伝子の発現量が周期的に変化すること(時計遺伝子の振動)によって体節形成(分節)を制御する「分節時計」が存在することが明らかになっている。しかし、ヒトにおいては体節形成期の胚の使用は制限されていることから、ほとんどのことが明らかにされていなかった。
研究グループはこれまでに、マウスやニワトリなどのモデル生物における中胚葉の分化とパターン形成について研究してきた。その成果をふまえ、試験管内(in vitro)でヒトの中胚葉形成を再現できるのではないかと考えた。また、ヒトにおいても分節時計が機能しており、振動する時計遺伝子の可視化と定量が可能であると考えた。
分節時計との関連が報告されていないシグナル経路を見出すことに成功
研究グループは今回、iPS細胞を用いて、胚発生を模した形で段階的にヒトPSMを誘導するin vitroの二次元/三次元分化系を確立した。すでにモデル生物を用いた胚発生研究によって、分節時計におけるシグナル伝達経路の活性変化が明らかになっていた。この実験系では、その活性変化を模した培養系で、PSMとそこから分化する組織を誘導した。
その結果、この in vitroのiPS細胞由来PSMにおいて、発現が大きく振動する遺伝子を複数同定した。また、PSMにおいて振動する遺伝子の1つである、HES7のレポーター細胞を樹立した。このレポーター細胞を用いて解析したところ、誘導したPSMにおいて、HES7遺伝子の発現が約5時間周期で振動することが確認できた。その際に、分節時計のメカニズムの重要な特徴である、遺伝子の発現が進行波の様に移動していく様子が観察できたという。
さらに、この実験系でマウスの未分節中胚葉を誘導し、in vitroにおけるマウスの分節時計が、実際の胚における周期と同じ2~3時間であることも示した。加えて、確立した誘導法を用いてHES7を振動発現させたヒト及びマウスのin vitro PSMを用いたRNAシーケンシング解析により、約200個の新規の同位相/逆位相振動遺伝子を同定し、これまで分節時計との関連が報告されていないシグナル経路を見出すことに成功。これにより、分節時計のメカニズムについての新しい知見が得られた。
また、ゲノム編集技術CRISPR/Cas9を用いて、椎骨分節異常(SDV)や脊椎肋骨異骨症(SCD)などで報告されている原因遺伝子に、疾患特異的な変異を持つiPS細胞を樹立した。これらの細胞株を、同研究で確立したin vitro誘導系を用いてPSMに誘導したところ、疾患に特異的な遺伝子変異が、分節時計の発現振動、振動の同調、分化へ与える影響を検証することができた。さらに、SDVやSCDの患者から樹立した iPS細胞を用いたPSM誘導でも、同様の分節時計の異常を検出することができた。CRISPR/Cas9を用いてこの疾患特異的な遺伝子変異を修正したところ、分節時計の異常な発現振動・周期・分化が一部正常に戻ることが確認されたという。
基礎的なヒト生物学の理解や先天性疾患などの異常な胚発生に関する知見をもたらす発見
今回の研究で確立された分節時計のin vitroモデルの確立は、ヒトの体節形成や分節メカニズムの理解について、1つのターニングポイントとなる成果と言える。ヒトの主要な発生過程については、倫理的な制約からこれまで立ち入ることができなかったが、今回の再現性の高いin vitroモデルにより、ヒトの中胚葉形成の研究のみならず、胚発生時期に関する疾患研究へ、多くの可能性がもたらされた。
さらに、iPS細胞を活用した人工発生学的アプローチは、ヒトだけでなく、その他の哺乳類や、は虫類の発生過程(体節形成など)の研究への可能性をも開くものだ。分節時計がなぜ、どのように種特異的であるのかといった課題の解明に貢献することが期待される。また、同モデルは、発生時間がどのようにして実際の発生プロセスを制御しているか、また、疾患や進化において、発生時間の制御メカニズムにおける異常や変化がどのように分節過程に影響を与えるかなどの問題を解決する一助となると考えられる。さらに、ヒトの通常の胚発生のみならず、先天性疾患のような異常な胚発生に関して知見を加えるものだと言える。
研究グループは、「本研究は、iPS 細胞を用いることによって、基礎的な生物学の問題を解明できるだけではなく、複雑な先天性疾患の病因に対して新たな知見を与えることのできる好例だ。本研究と今後の研究が、基礎的なヒト生物学の理解をさらに深めることを切に願う」と、述べている。
▼関連リンク
・京都大学 研究成果



