患者のがん組織を網羅的に遺伝子解析、特徴を探索
新潟大学は3月3日、卵巣成熟嚢胞性奇形腫から発生したがんに対する網羅的な遺伝子解析を行い、がんの診断や治療効果を予測する可能性のある分子として「XCL1」を同定したと発表した。これは、同大大学院医歯学総合研究科産科婦人科学分野の榎本隆之教授、吉原弘祐助教、田村亮助教らの研究グループを中心とした国内多施設共同研究によるもの。研究成果は、Nature publishing group の「Oncogene」に掲載されている。
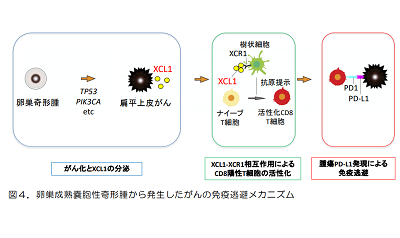
画像はリリースより
卵巣成熟嚢胞性奇形腫は、最も頻度が高い良性の卵巣腫瘍で、1~2%の割合でがん化するといわれている。有効な治療法が確立していないため、がんが進行した状態で見つかると非
常に予後が悪い。まれな疾患で、術前に診断することも難しく、臨床検体を用いた研究やがん化のメカニズムは依然として不明だ。また、卵巣成熟嚢胞性奇形腫から発生したがんの約80%が扁平上皮がんである。卵巣成熟嚢胞性奇形腫は、別の言い方で皮様嚢腫(デルモイドシスト)と呼ばれるように、ほとんどの症例が皮膚のような上皮を含んでおり、その皮膚様組織からがんが発生することが多いと考えられていた。
そこで研究グループは、卵巣成熟嚢胞性奇形腫から発生したがんと診断された患者に研究参加の同意を得た上で、手術時に採取したがん組織の遺伝子解析を実施。具体的には、採取した組織からDNAおよびRNAを抽出し、その塩基配列を次世代シーケンサーで網羅的に読み取り、遺伝子異常(遺伝子変異、コピー数変異、融合遺伝子など)の同定や網羅的遺伝子発現解析を行った。また、遺伝子発現データに基づいた同疾患の特徴を明らかにするため、「The Cancer Genome Atlas(TCGA)Data Portal」、「Gene Expression Omnibus(GEO)」に登録されているさまざまな臓器から発生した2,316例のがんの遺伝子発現データと比較。そして、網羅的な遺伝子解析で同定した結果について、免疫染色を用いて追加検討を行った。
XCL1発現によるPD-L1発現、がん免疫療法が有効の可能性
解析の結果、同疾患においてがん抑制遺伝子であるTP53、がん遺伝子であるPIK3CAが高頻度に変異していることが明らかになった。また、発がんやがんの進展に重要な経路であるPI3K-AKTmTOR pathwayやCell cycle pathwayに関わる遺伝子が、高頻度に遺伝子異常を起こしていることもわかった。さまざまな臓器から発生した扁平上皮がんと遺伝子発現パターンを比較したところ、これまで発生母地として有力と考えられていた皮膚から発生した扁平上皮がんよりも、肺から発生した扁平上皮がんに類似していることが確認された。
さらに、同疾患と他部位から発生した扁平上皮がんの遺伝子発現を比較し、発現差が顕著な遺伝子として「XCL1」を同定。XCL1はリンパ球の活性化に重要な役割を持っていることが報告されている遺伝子である。そこで、免疫療法の効果を予測する有力なバイオマーカーである、CD8リンパ球浸潤、腫瘍でのPD-L1発現を確認したところ、XCL1発現は両方と有意に相関していることがわかった。つまり、XCL1高発現により、CD8リンパ球浸潤が起こり、それに反応してがんがPD-L1を発現し、免疫逃避状態を呈していると推察されるという。
今回の研究の最も重要な点は、卵巣成熟嚢胞性奇形腫から発生した扁平上皮がんが、特徴的XCLを高発現しており、免疫逃避に関与している可能性が明らかになったことである。「PD1-PDL1による免疫逃避状態にある予後不良な本疾患に対して、PD1/PDL1抗体を用いた免疫療法が有効であろうと考える。今後、細胞株や動物モデルを用いて本研究成果を検証し、また多施設共同研究によって、卵巣成熟嚢胞性奇形腫から発生した扁平上皮がんの臨床病理学的データを大規模に集積して本研究成果を検証することで、本疾患に対する免疫療法の適応拡大を目指す」と、研究グループは述べている。
▼関連リンク
・新潟大学 研究成果




