細胞内異常タンパク質は「オートファジー」、細胞外は?
千葉大学は2月18日、血液中など細胞外に生じた異常タンパク質を細胞が自ら取り込み分解・除去する仕組みを発見したと発表した。この研究は、同大大学院理学研究院の板倉英祐助教らの研究グループによるもの。研究成果は、「Journal of cell biology」に掲載されている。
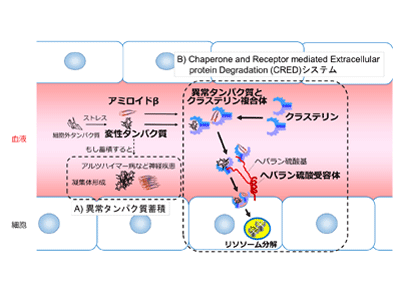
画像はリリースより
人の体の中には約2万種類のタンパク質が存在し、それぞれがさまざまな機能を保つことで生体恒常性が維持されている。血液中のタンパク質は細胞間の情報伝達や物質輸送の機能を担っているが、タンパク質は熱ストレスや老化に伴い変性し、機能を失った変性タンパク質となる。特に、細胞の外はタンパク質にとっては過酷な環境で変性しやすく、変性したタンパク質が蓄積すると、正常な生体内の機能を阻害する。例えば、異常タンパク質の1つであるアミロイドβは、蓄積することでアルツハイマー病の発症を引き起こすと考えられている。細胞の中の異常タンパク質を分解する仕組みは、オートファジーと呼ばれ、研究が盛んに進められているが、細胞の外にある異常タンパク質を細胞が除去する仕組みについては、これまで詳しくわかっていなかった。
細胞外異常タンパク質は、クラステリン<へパラン硫酸受容体<リソソーム分解
今回、研究グループは、クラステリンという細胞外分子シャペロンに着目して解析を実施。その結果、細胞外で変性した異常タンパク質が生じると、クラステリンが特異的に結合して捕まえることを見出した。また、クラステリンが取り込まれると細胞が蛍光を発する手法を開発し、これを用いたことで、クラステリンと異常タンパク質の複合体を細胞が取り込み、分解酵素を含む細胞小器官リソソーム内に運ばれて分解されることも判明した。
続いて、研究グループ独自のクラステリン取り込み細胞が蛍光を発する手法と、CIRSPRによる遺伝子欠損細胞を組み合わせ、クラステリン分解能を欠損した変異体細胞を探索。その結果、ヘパラン硫酸受容体の同定に成功した。同受容体は、線状の多糖類であるヘパラン硫酸基をもつ細胞表面の受容体タンパク質であり、増殖因子やウイルスの受容体となることが知られていたが、今回、異常タンパク質の受容体になっていることが初めて実証された。
さらに詳細な解析から、細胞外の異常タンパク質が細胞に取り込まれるまでの一連の除去システムが明確になり、クラステリン-異常タンパク質複合体は、細胞表面のヘパラン硫酸受容体との直接結合によって捕らえられ、細胞内に取り込まれていることが明らかになった。また、アルツハイマー病のリスク因子であるアミロイドβと結合したクラステリン複合体も、同様の除去システムによって分解でき、この除去システムはほとんどの細胞種がもつ普遍的な機能であることがわかった。研究グループは、このシステムを「Chaperone and Receptor mediated Extracellular protein Degradation(CRED)」と名づけた。研究グループは、「このCREDシステムを応用することで、細胞外異常タンパク質の蓄積が誘因となる疾患治療への応用が期待できる」と、述べている。
▼関連リンク
・千葉大学 ニュース



