雌型の性決定が行われるための遺伝子発現制御の機序について研究
京都大学は2月14日、マウスを用いた実験で、生殖細胞が雌型に性決定し、卵母細胞へと分化する仕組みを解明したと発表した。これは、同大高等研究院ヒト生物学高等研究拠点(ASHBi)拠点長の斎藤通紀教授(兼:京都大学大学院医学研究科教授、京都大学iPS細胞研究所連携主任研究者)、同ASHBiの長岡創特定研究員らの研究グループによるもの。研究成果は、米国科学誌「Science」のオンライン速報版に掲載されている。
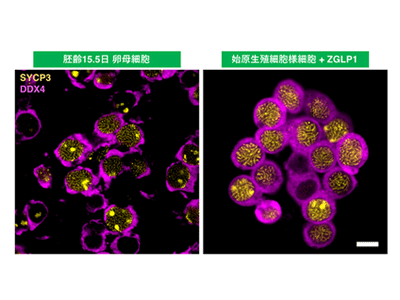
画像はリリースより
生殖細胞は、体の細胞の中で唯一、次世代へとゲノム・エピゲノム情報を伝えることができる細胞だ。胎児期の早い段階で他の体細胞とは分けられて発生し、発生直後は生殖細胞の性は決まっておらず(始原生殖細胞と呼ぶ)、胎児の成育が進むにつれて、雄の個体では精子を作るためのプログラムが活性化され、雌の個体では卵子を作るためのプログラムが活性化される。しかし、これらの生殖細胞が性特異的なプログラムを活性化する分子機構は不明だった。
近年、生殖細胞の発生過程を理解するための新たなアプローチとして、多能性幹細胞から生殖細胞を誘導し、その発生を培養ディッシュ上で再現することにより、生殖細胞の発生・分化の機構を詳細に解析できる実験基盤が開発された。この実験基盤を活用し、研究グループはこれまでに骨形成因子(BMP)と、ビタミンAの代謝産物であるレチノイン酸の2つの液性因子により、生殖細胞から卵母細胞への分化が誘導できることを発見していたが、その作用機序は不明だった。
そこで研究グループは、マウス卵母細胞への分化を誘導する転写因子を同定し、雌型の性決定が行われるための遺伝子発現制御の機序を明らかにすることを目的として研究を行った。
Zglp1遺伝子欠損マウスは不妊に至ることが判明
まず、卵母細胞分化を誘導する候補遺伝子を絞るために、マウス胎児生体内における性決定直後の卵母細胞および、BMPとレチノイン酸で誘導された培養ディッシュ上の卵母細胞の遺伝子発現情報を用いて、8個の候補遺伝子を選出。次に、それらの遺伝子を任意のタイミングで発現できるES細胞を作製し、始原生殖細胞様細胞へと分化させた細胞にて候補遺伝子を人工的に発現させ表現型を解析した。すると、胎児期の卵母細胞にて起こる減数分裂を誘導できることがわかった。その後、誘導に用いる遺伝子を1つずつ減らしたところ、Zglp1を発現させるベクターを除くと、卵母細胞誘導能が極端に落ちること、そして、Zglp1を単独で発現させるだけで90%以上の細胞を卵母細胞へと誘導できることが明らかになった。
Zglp1の遺伝子欠損マウスを解析したところ、胎児期で減数分裂への移行に支障があり、胚齢17.5日の卵巣では、生殖細胞の数が正常マウスの0.6%以下に激減、そして生後8日目までに完全に消失し、その結果、Zglp1遺伝子欠損マウスは不妊に至ることが判明した。
その後、Zglp1とBMP・レチノイン酸シグナルとの関係や、卵母細胞形成に必要と知られている遺伝子群との関係性を網羅的に解析したところ、Zglp1の発現はBMPにより誘起され、BMPの刺激で誘起される卵母細胞形成関連遺伝子の95%以上がZglp1にその発現を依存していることが明らかになった。そして、BMPとZGLP1が軸となって卵母細胞運命の基盤を構築するのに対し、レチノイン酸シグナル経路は運命決定の促進と補助、そして、PGCプログラムの抑制化という役割を担っていることが明らかになった。また、ZGLP1は抑制的なエピゲノム状態を有している遺伝子群を、より優先的に活性化させることも判明した。
不妊症の原因解明、先天性の染色体疾患の発症機序の解明につながる可能性
今回の研究成果により、今まで不明だった卵形成始動のための遺伝子制御機構が明らかとなり、また、多能性幹細胞から転写因子のみを用いて卵母細胞を誘導することが可能であることが証明された。今後は機能的な卵子ができるための分子制御機構のさらなる解明、また、精子形成を開始する雄型の性分化の仕組みの解明を目指すという。
研究グループは「ヒト始原生殖細胞様細胞から卵母細胞そして卵子へと分化誘導する方法論の開発を推進する。将来的には不妊症の原因解明、先天性の染色体疾患の発症機序の解明など、生殖医療の発展に役立つことが期待される」と、述べている。
▼関連リンク
・京都大学 研究成果




