脳内のアミロイド除去に成功しても症状が改善されないのはなぜか
東京医科歯科大学は1月22日、アミロイドベータ細胞外凝集の出現前の超早期段階に生じる細胞死が、その後のアルツハイマー病態進展の鍵を握ること、また、この細胞死を標的とする治療法(発症後にも適応可能)の開発が可能であることを実験的に示したと発表した。この研究は、同大難治疾患研究所/脳統合機能研究センター神経病理学分野の岡澤均教授の研究グループが、東京都健康長寿医療センター、名古屋大学、自治医科大学、慶応義塾大学、国立精神神経医療研究センター、国立シンガポール大学、バロー神経学研究所などのグループとの共同研究として行ったもの。研究成果は、国際科学誌「Nature Communications」にオンラインで掲載されている。
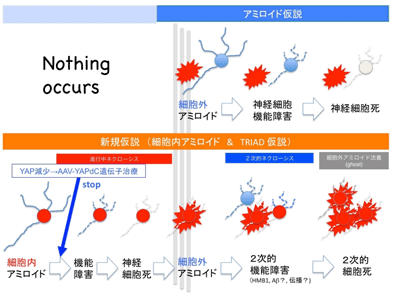
画像はリリースより
アルツハイマー病をはじめとする神経変性疾患の病理学的な特徴は、細胞の内外に異常タンパク質が蓄積することだ。アルツハイマー病では、細胞外にアミロイドベータ(以後、アミロイドと略称)と呼ばれる異常ペプチドが沈着する老人斑と、細胞内にタウタンパク質が凝集する神経原線維変化の2つが起こることが知られている。これまで数々の治療法が試みられてきたが、十分な有効性を示すものは得られていない。特に、約15年前からアミロイドに対する抗体医薬品の臨床試験が国際的な規模で行われてきたが、脳内のアミロイド除去に成功したものの、患者の症状は改善が見られないことも予想外の知見として得られた。このため、発症後から治療を開始するのでは既に遅く、発症前にアミロイド抗体療法を開始する、あるいは、脳内の細胞外アミロイド凝集が起きる以前の超早期(Phase 0)に生じる脳内分子変化を解明して、新たな分子標的に対する治療を開発する必要があると考えられるようになってきた。
細胞外アミロイド蓄積以前の早期段階からネクローシスが起きていた
研究グループは先行研究で、脳内細胞外アミロイド凝集前にリン酸化の異常変動を示すタンパク質MARCKSを同定し、リン酸化MARCKS(pSer46MARCKS)が細胞外アミロイドの周囲にある変性神経突起に存在することを報告した。また、pSer46MARCKSの上流シグナルがHMGB1であることを示し、MARCKSのリン酸化を誘導する細胞外分子HMGB1を標的とする抗体治療法がアルツハイマー病の発症を予防することを報告してきた。
HMGB1はネクローシスというタイプの細胞死を起こした時に放出されることが知られている。そこで、今回研究グループは、患者の髄液中のHMGB1を測定。その結果、アルツハイマー病として診断される時期の髄液よりも、軽度認知障害(MCI)の時期の患者の髄液の方が、HMGB1がより高値であることを見出した。このことは発症前にすでに細胞死が活発に起きていることを示唆している。
続いて研究グループは、アルツハイマー病の2種類のモデルマウスを用いて、今回の研究で開発したpSer46MARCKS抗体で進行中の神経細胞ネクローシスを検出する技術によって、現在進行形のネクローシスを定量。すると、認知機能障害を起こすより前に、なおかつ、細胞外アミロイド蓄積が見られる前から、ネクローシスが盛んに起きていることが明らかになった。現在進行形ネクローシスは、発症前にピークがあるものの、発症後にも続いているということも示された。
遺伝子治療によるYAP補充でモデルマウスの病態改善
また、ゲノム編集技術を用いてアルツハイマー病遺伝子変異を導入したヒトiPS細胞から分化作成したヒト・アルツハイマー病ニューロンの詳細な観察から、このようなネクローシスは細胞内アミロイドがYAPと呼ばれるタンパク質を巻き込んで、YAPの細胞生存維持作用が奪われるために生じる新しいタイプのネクローシス(TRIAD)であることがわかった。
さらに、ネクローシスを引き起こすYAP機能障害を正常化する目的で、遺伝子治療によるYAP補充をアルツハイマー病モデルマウスに対して実施。その結果、TRIADネクローシスの抑制、認知機能改善、そして、細胞外アミロイド蓄積の抑制が観察された。
今回の研究で、1)細胞内アミロイド蓄積に始まるネクローシスの結果として細胞外アミロイド凝集が起きること、2)細胞内アミロイド蓄積に起因するネクローシス過程およびネクローシスを起こした細胞の周辺神経細胞が起こす二次的細胞死過程が、神経機能障害を引き起こしていること、3)細胞内アミロイド蓄積がトリガーするネクローシスはYAP機能低下に起因するTRIADであること、4)YAP機能回復を基盤とする遺伝子治療等の治療開発が今後可能であること、5)髄液HMGB1量はアルツハイマー病の発症前分子マーカーとして開発しうる可能性があること、が、示された。研究グループは、「本研究を通じて、細胞外アミロイド凝集を最上流の原因と考えるアミロイド仮説を訂正する必要性が強く示唆された」と、述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース



