全身のさまざまな臓器に炎症による障害が起きる原因不明の難病
東京理科大学は12月20日、肝臓、すい臓、腎臓などの臓器や、血管、涙腺、唾液腺など、全身の様々な組織に腫れや炎症を生じる原因不明の難病「IgG4関連疾患」について、臓器に強い炎症が生じるメカニズムを明らかにしたと発表した。この研究は、同大生命医科学研究所分子病態学研究部門の久保允人教授らの研究グループが、慶應義塾大学医学部リウマチ・膠原病内科の竹内勤教授、理化学研究所生命医科学研究センター免疫シグナル研究チームの斉藤隆チームリーダー、北里大学医学部膠原病・感染内科学の山岡邦宏教授と共同で行ったもの。研究成果は、「International Immunology」にオンライン掲載されている。
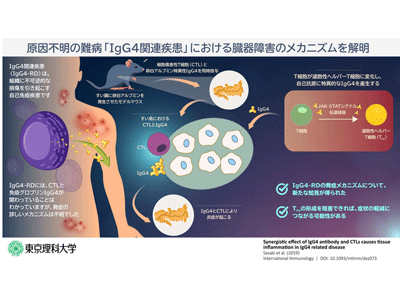
画像はリリースより
IgG4関連疾患は、全身のさまざまな臓器に炎症が起き、それによって痛みや機能の低下などの症状が出ることが特徴。障害が起きる臓器は患者によって異なるが、脳で起きればホルモンの異常が生じて頭痛や尿崩症などにつながる。涙腺や唾液腺で起きれば、目の周りや顎に腫れが出る(ミクリッツ病)。肺や腎臓、すい臓などの臓器に発生すると、臓器の機能が低下するほか、増殖して浸潤した形質細胞ががんと誤診されることもある。
2001年、すい臓にできる腫瘤や黄疸などを主症状とする自己免疫性膵炎の患者で、血液中のIgG4の濃度が著しく高くなっていることが報告され、それをきっかけに複数の疾患が、IgG4に着目して捉え直されるようになった。現在では、臓器の炎症に加え、血中のIgG4濃度の上昇、IgG4陽性形質細胞の臓器への浸潤が見られる疾患をひとまとめにして、IgG4関連疾患と呼ぶようになっている。治療には免疫反応を抑えるステロイド剤が主に使われるが、効果が十分でないケースや、薬をやめると再発するケースも少なくなく、疾患が起きるメカニズムの解明と、それに基づいた新しい治療法の開発が待たれている。
IgG4と細胞傷害性T細胞の相乗効果で炎症が増悪
IgG4関連疾患のメカニズムの解明が進まなかった原因のひとつは、適切な動物モデルが得られなかったことにある。動物実験で多く使われるマウスは通常、IgG4を持たないからだ。そこで研究グループは今回、卵アレルギーの原因物質のひとつで、免疫反応のシミュレーションに良く使われるタンパク質の卵白アルブミン(OVA)をすい臓の細胞膜で強制的に発現させたマウス(RIP-mOVAマウス)を用いた実験系を組んだ。このマウスに対して、OVA特異的細胞傷害性T細胞(OT-I細胞)と、OVA特異的ヘルパーT細胞(OT-II)、遺伝子組み換えにより作成したOVA特異的ヒトIgG4抗体(以下、ヒトIgG4抗体)を組み合わせて使用することで、抗原特異的なIgG4抗体とT細胞がIgG4関連疾患にどのように関わっているかを検証する動物実験モデルを確立することに成功した。
実験の結果、ヒトIgG4抗体を単独でRIP-mOVAマウスに投与しただけでは、炎症反応は起きなかった。IgG4関連疾患では、腫れた臓器に細胞傷害性T細胞が集積していることが報告されているが、OT-Iを単独投与しても激しい炎症反応が起きることはなかった。ところが、ヒトIgG4抗体とOT-I細胞を一緒に投与すると、RIP-mOVAマウスのすい臓で激しい炎症が起きることが確認された。さらにこのとき、すい臓に加えリンパ節では、樹状細胞の集積が見られた。一方で、ヒトIgG4抗体が働かないようにIgG4の受容体(FcγR)をブロックすると、OT-I細胞の活性化が見られなくなった。これらのことから、ヒトIgG4抗体の存在によって樹状細胞の働きが促進され、OT-I細胞が活性化されやすくなること、この活性化が病変臓器の激しい炎症の原因となっている可能性が高いことが示唆された。
濾胞性ヘルパーT細胞の機能抑制で治療できる可能性
続いて、OT-I細胞とOT-II細胞をRIP-mOVAマウスに投与したところ、OVAを抗原とする抗OVA抗体が作り出され、IgG4を同時投与した場合と同様、OT-I細胞に起因した激しい炎症反応を引き起こすこともわかった。抗体を作り出す免疫細胞は、「濾胞性ヘルパーT細胞」が放出するインターロイキン4(IL-4)によって制御されている。IL-4の働き、または濾胞性ヘルパーT細胞の機能そのものをブロックすると、抗体を作る細胞の機能に加え、OT-I細胞による炎症反応が抑制された。このことは、OT-I細胞の働きもまたIL-4によって制御されていること、また、OT-I細胞の働きを抑え、臓器の炎症を緩和する新たな治療薬として、濾胞性ヘルパーT細胞の機能を抑制する薬剤を利用できる可能性があることを意味する。実験では、濾胞性ヘルパーT細胞の形成を阻害する免疫抑制剤(ヤヌスキナーゼ阻害剤の一種、トファシチニブ。関節リウマチ等の治療薬として使用されている)の投与により、RIP-mOVAマウスのすい臓の炎症を改善させることができた。
今回、IgG4関連疾患の病変臓器で激しい炎症反応が起きるメカニズムの一端が解明されたことにより、これまでになかった新しい治療戦略の可能性が複数提示された。研究グループは、「疾患の発生と増悪のメカニズムを検証するために有効な動物実験モデルが確立できたことと合わせて、近い将来、新たな治療法の開発につながることが期待される」と、述べている。
▼関連リンク
・東京理科大学 プレスリリース



