肺の構造は極めて複雑なため、従来法では臓器再生は困難だった
11月13日、従来の胚盤胞置換法において移植する多能性幹細胞側(ドナー)、移植される側(ホスト)の双方を改良させることで機能的な肺臓器再生が実現可能であることを立証したと、コロンビア大学のCardoso研究室の森宗昌研究員(instructor:研究チームリーダー)と東京大学(Stanford大学教授を兼任)の中内啓光特任教授は、東京大学医科学研究所を通して発表した。研究成果は米国科学雑誌「Nature Medicine」のオンライン版で公開されている。
画像はリリースより
世界中で何百万人もの人々が苦しんでいる難治性呼吸器疾患を克服するような画期的な治療法はいまだない。慢性閉塞性肺疾患や肺繊維症、先天性の肺疾患、重症肺炎後の重度呼吸器不全などによりひどく壊れてしまった肺は、元通りに戻す方法がなく、唯一の根本治療法は肺移植だけだが、ドナー肺は絶対的に不足しているのが現状。もしドナーの細胞を使って肺をもとに戻すことができれば大きな医学的前進といえるが、肺は大変複雑な構造をもつため、いかなる生物工学的な手法を用いても肺臓器再生は極めて困難と考えられてきた。今回研究グループは、ユニークな肺無形性モデルマウスを作製し、発生段階初期に新規培養系を用いたドナー細胞を移植することで、機能的な肺臓器の再生に取り組んだ。
新たな胚盤胞置換法と新たな培養系を組み合わせてドナー細胞由来肺を作成
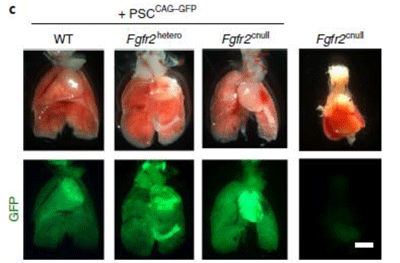
研究グループは、肺形成に必須のFgfr2遺伝子を、Shhプロモーターを用いて内胚葉特異的に欠損させ、他の臓器にあまり影響を及ぼさず、肺だけがつくられない条件付き(Conditional)のモデルマウスを作製し、その表現型を「胚盤胞置換法」で補完することを目指した(Conditional blastocyst complementation:CBC)。胚盤胞置換法は、ホストの動物に発生段階初期(胚盤胞形成期)にドナー細胞を移植する方法。ホスト動物の発生プログラムをドナー細胞は利用し、ホスト動物由来の細胞とドナー細胞が共存(キメラ形成)しながら発生していく。
このマウスは産まれた直後、肺がないため、呼吸ができずに死んでしまう。この致死的な状態を救済するために、多能性細胞(ドナー細胞)を胎児発生の初期、胚盤胞形成期に移植した。研究グループは、さまざまな条件検討の結果、キメラ形成能が高い多能性幹細胞を極めて高効率に維持する新規の培養系(a2i/VPA/LIF)を開発。そこで培養されたドナー細胞を胚盤胞形成期に移植することで、ドナー細胞由来の肺を高効率に作製できることを証明した。
肺無形成モデルマウスで肺臓器を高効率に補完、成体まで問題なく生存
この再生肺は、肺の機能検査でコントロールである野生型キメラマウスと同等の肺機能を維持し、その遺伝子改変マウスは生後から成体(生後80日)まで、全く問題なく、生きのびることができるということが証明された。さらに研究グループは、内胚葉特異的にBeta-Cateninを欠損させることで、肺と気管支が発生しない、別の肺無形成マウスモデルも作製。このマウスモデルにおいても、新規培養系で培養されたドナー細胞を移植すると、肺と気管支の両方が補完され、マウスが成体まで生きることが証明された。すなわち、構造が複雑で細胞種が多い肺のような臓器でも、CBCと新規培養系を組み合わせることで、機能臓器の再生が可能であることが証明された。
これまでは、肺という臓器は、形態的に複雑かつ細胞の種類が多いため、再生が極めて困難と考えられてきた。この課題を克服するために、研究チームは森研究員が主導となり、ドナー細胞側とホストサイド双方において臓器再生技術を見直し、肺臓器再生のために最適化を行ってきた。その結果、再現性よく、かつ、高効率に肺臓器を再生する技術基盤の確立に成功した。研究グループは、「今後この技術基盤をさらに応用して、異種間への応用や、難治性肺疾患の克服のための病態動物モデルの開発、大動物における肺臓器再生への応用を期待している」と、述べている。
▼関連リンク
・東京大学医科学研究所 プレスリリース



