AKIにおけるcGAS-STING経路の関連などを検討
東京大学医学部附属病院は10月30日、急性腎障害(acute kidney injury:AKI)におけるミトコンドリアの機能異常とそれに引き続く炎症誘導のメカニズムを解明したと発表した。この研究は、同大医学部附属病院の前川洋医師、同大大学院医学系研究科の稲城玲子特任教授らの研究グループによるもの。研究成果は「Cell Reports」オンライン版で掲載された。
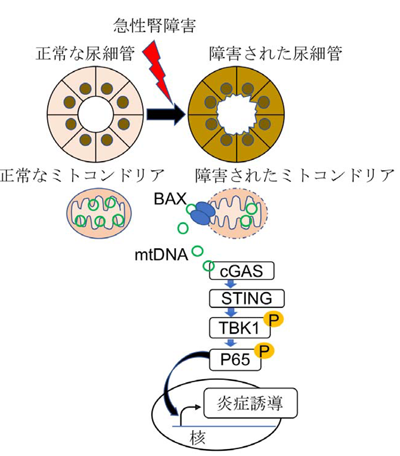
画像はリリースより
AKIは、さまざまな原因で急速に腎機能が悪化する病気。尿が作られなくなり、本来は尿から排泄されるさまざまな物質が体内に貯留することで、心不全や電解質異常といった尿毒症症状が起こる。重症例では透析治療が必要になり、腎機能改善後も将来的に腎機能が不可逆的に低下した慢性腎臓病や腎臓が完全に廃絶する末期腎不全に進展する可能性が高まることが知られている。
また、AKIでは腎臓を構成する細胞の一種である近位尿細管細胞のミトコンドリア障害と炎症反応が誘導されることが以前から知られていた。加えて細胞質内のDNAを認識し自然免疫反応を引き起こすcyclic GMP-AMP synthase(cGAS)- stimulator of interferon genes(STING)経路が近年発見され、注目を集めている。そこで研究グループは今回、AKIにおける近位尿細管細胞のミトコンドリア障害および炎症誘導とcGAS-STING経路の関連について検討した。
新たなAKI治療方法開発にも期待
同研究では、マウスに抗がん剤シスプラチンを投与するAKIモデルを用いた。シスプラチンを投与したマウスではAKIが生じ、腎臓内でのcGAS-STING経路の活性化や炎症性サイトカインの発現が上昇していることが明らかになった。また、AKI患者の腎組織標本を用いた検討でも、cGAS-STING経路の活性化が示唆される結果が得られたという。
次に、STINGの発現を抑制したSTINGノックアウトマウスでは、シスプラチンによる腎機能障害、炎症反応が改善しており、STING阻害薬においても同様の結果が認められた。近位尿細管細胞にシスプラチンを添加しフラックスアナライザーおよびフローサイトメトリーを用いて検討したところ、ミトコンドリア機能障害、ミトコンドリア外膜の電位低下が確認されたという。詳細な検討を行った結果、シスプラチンを添加した近位尿細管細胞ではミトコンドリアDNAが細胞質に漏出し、cGAS-STING経路を活性化し、炎症が誘導されていることがわかった。加えて、このミトコンドリアDNAはミトコンドリア外膜上のアポトーシスに関係する分子とし知られるBAXが流出路となり漏出していると考えられたとしている。
今回の研究により、AKIでは、近位尿細管細胞においてミトコンドリア障害が起き、それに引き続くミトコンドリアDNAの細胞への漏出が生じ、cGAS-STING経路の活性化を介した尿細管炎症が引き起こされることが明らかとなった。さらにこの尿細管炎症が病態の進展に関与することもわかった。したがって、この経路を抑制することで将来的に新たなAKI治療方法開発が期待される。研究グループは、今回の成果を基盤とし、今後はcGAS-STING経路の他の腎疾患モデルにおける関与を探索し、この経路をターゲットとした治療法の開発に取り組んでいく予定だとしている。
▼関連リンク
・東京大学医学部附属病院 プレスリリース



