ポドプラニンとCLEC-2の結合を阻害する化合物探索
東海大学は9月27日、がん転移阻害薬の開発を加速させる画期的な評価システムの構築に成功したと発表した。この研究は、同大医学部医学科外科学系救命救急医学の猪口貞樹 前教授(現客員教授)、渡邊伸央助教、先進生命科学研究所を中心とした研究グループによるもの。研究成果は「PLOS ONE」に掲載されている。
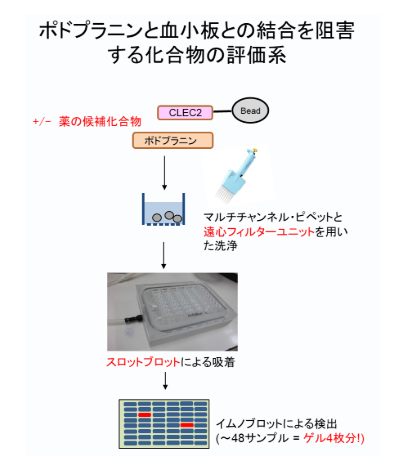
画像はリリースより
日本人の死因第1位はがん、再発や転移により死亡率が高まっていると考えられている。多くのがん組織において、ポドプラニンと呼ばれる膜タンパク質の発現が上昇しており、この値が高くなるほど、切除手術後の再発・転移のリスクも高まることがすでに報告されている。
ポドプラニンは通常、リンパ管の内皮細胞など、限られた組織でのみ発現し、がんの悪性度の指標にもなっている。がんの再発・転移は、ポドプラニンと血小板の「CLEC-2」と呼ばれるタンパク質が結合し、血小板の活性化が誘導されることに起因しているとみられており、ポドプラニンと血小板の結合を阻害できる化合物が見つかれば、がんの転移防止薬となり得る。そこで、しかし、現在のところ、このような作用機序を持つ化合物は明らかになっていない。
1度に48サンプルを、従来法より迅速に評価可能
研究グループは遺伝子組み換え法により、目印となるタンパク質を融合させたCLEC-2とポドプラニンを溶液中で結合反応させた後、この目印を利用してCLEC-2とポドプラニンの複合体を沈降させる「プルダウン・アッセイ」という評価システムを構築した。結合反応時に共存させた化合物がCLEC-2とポドプラニンとの結合を阻害すれば、ポドプラニンの沈降が抑制されることになる。
従来のプルダウン・アッセイでは、1サンプルごとに洗浄等の操作をするため、薬の候補化合物評価(スクリーニング)には不向きだった。しかし今回構築したこの評価システムでは、一度に48サンプルを評価することが可能で、従来の方法に比べて約5~10分の1の速さで正確に候補化合物を探索することができる。現状、世界中から報告されている評価システムの中で最も迅速かつ測定精度の高い評価システムであるといえる。
「今回開発した評価システムにより、従来は開発が難しかったがん転移抑制薬の研究開発が一挙に加速され、人類の悲願である「がん撲滅」への道がさらに大きく開けると期待される」と、研究グループは述べている。
▼関連リンク
・東海大学 ニュース




