「遺伝子検査で見つかった変異は疾患の原因か」を判定するのが困難
京都大学は9月24日、家族性地中海熱の新たな診断方法を開発したと発表した。この研究は、同大医学研究科の西小森隆太准教授(現:久留米大学准教授)、八角高裕准教授、同大医学部附属病院の田中孝之医員、同大医学研究科の芝剛博士課程学生(現:天理よろづ相談所病院)らの研究グループによるもの。研究成果は、国際学術誌「Journal of Allergy and Clinical Immunology」のオンライン版に掲載されている。
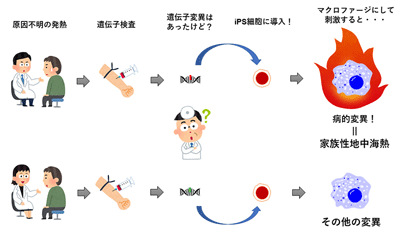
画像はリリースより
家族性地中海熱は激しい腹痛・胸痛を伴う発熱発作を周期的に繰り返す疾患。日本国内の患者数は500人程度とされている。治療薬としては「コルヒチン」が有効だが、同剤が無効または副作用で使えない場合には、発熱物質であるインターロイキン1βに対する抗体製剤が有効である。炎症に関係するタンパク質「パイリン」の異常が原因とされており、遺伝子検査が診断の助けとなるが、病気との関連性が不明な遺伝子変異が見つかることがあり、その変異が患者の発熱の原因になっているのかを判断するのが困難だった。
研究グループは以前から自己炎症性疾患の研究を行っており、クリオピリン関連周期熱症候群などで研究成果を報告している。また、iPS細胞研究所とも協力し、iPS細胞を用いた免疫疾患の研究を行ってきた。そこで今回、これまでの技術を応用し、家族性地中海熱の診断法を開発することを目的として研究を開始した。
インターロイキン1βの分泌を評価することで、より正確な診断が可能に
研究グループは、家族性地中海熱の患者から血液を提供してもらい、その中の単球をマクロファージへ変化させた。そのマクロファージに対して、MEFV遺伝子により作られるタンパク質であるパイリンを活性化させるクロストリジウム毒素を投与したところ、家族性地中海熱患者のマクロファージでは健常者のマクロファージよりも発熱物質であるインターロイキン1βを過剰に分泌し、その分泌はコルヒチン投与により抑制された。これは、家族性地中海熱の患者の症状と合致するもので、マクロファージこそが家族性地中海熱の病態の鍵となる細胞である可能性を初めて見出した。
さらにiPS細胞研究所の協力のもと、患者の血液細胞からiPS細胞を作成しマクロファージへ変化させたところ、インターロイキン1βの過剰な分泌が再現された。次に、健常者由来iPS細胞へ種々の変異MEFV遺伝子を人工的に導入し、その後マクロファージへ変化させてインターロイキン1βの分泌を評価することで、個々のMEFV遺伝子変異が疾患の原因となるのかを判定する方法を開発。これにより、家族性地中海熱のより正確な診断が可能となり、患者に適切な治療が提供されることが期待される。
今回の研究成果により、家族性地中海熱の研究がさらに加速し、遺伝子変異の効果を患者の血液がなくとも実験室で判定できることが期待される。研究グループは、「ひとつひとつの変異の判定結果を蓄積・公開することにより、世界中の家族性地中海熱の診断に悩む医師、患者に貢献できると考えている。また、家族性地中海熱の第一選択薬であるコルヒチンは、マクロファージからの発熱物質の分泌を抑制することができた。この細胞を使うことで、効果や副作用の点でより優れた治療薬候補の探索も進めていきたい」と、述べている。
▼関連リンク
・京都大学 研究成果




