多機能性幹細胞から、全能性の謎解明へ
理化学研究所は8月9日、マウスの多能性幹細胞を初期化した後に分化させることで、着床可能な胚盤胞様の構造を誘導することに成功したと発表した。この研究は、理研生命機能科学研究センター網膜再生医療研究開発プロジェクトのコーディ・カイム基礎科学特別研究員、大阪医科大学薬理学教室の友田紀一郎講師らの共同研究グループによるもの。研究成果は、米科学雑誌「Stem Cell Reports」のオンライン版に掲載されている。
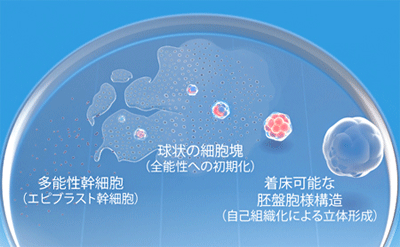
画像はリリースより
哺乳類の受精卵が細胞分裂(卵割)を繰り返すと、胚盤胞と呼ばれる袋状の構造が作られる。胚盤胞では、将来胎盤となる栄養外胚葉と体となる内部細胞塊の2種類が分化し、着床に向けた準備が進められる。内部細胞塊は「多能性」の幹細胞だが、受精卵の特徴である「全能性」を持たないため、胚盤胞より発生の進んだ細胞から胚盤胞そのものを作ることには、これまで成功していなかった。
研究グループはこれまで、マウスの着床後のエピブラストから樹立した多能性幹細胞(エピブラスト幹細胞:mEpiSC)が、特定の培養条件下で胚盤胞に似た半球状の構造を形成することを見出していた。
多能性幹細胞から胚盤胞を誘導する手法を開発
今回の研究では、受精卵の全能性や胚盤胞の着床など哺乳類の発生に必須である生命現象を解明するための実験系として、多能性幹細胞から胚盤胞を誘導する手法の開発を行った。
これまでの培養条件をさらに工夫し、BMP4などの増殖因子や、SMAD2/3細胞内シグナル伝達因子の阻害剤などを、2段階に分けて培養液に添加することで、胚盤胞により近い袋状の構造が7日目までに出現することを確認。この構造は、薬剤添加後5.5日目に培養液中に小さな球状の細胞塊として浮遊し始めたものが、自律的に成長・変形したものだったという。同研究グループは、mEpiSCから誘導されたこの構造を、「誘導性胚盤胞様嚢胞」を意味するiBLC(induced blastocyst-like cyst)と名付けた。
次に、iBLCの誘導を引き起こす分子機構を調べるため、mEpiSCからiBLCが形成されるまでの間に、全能性や細胞分化に関わる遺伝子の発現がどのように変化するかを観察。その結果、マウス2細胞期の全能性を示すMERVLレポーター遺伝子は、mEpiSCでは発現せず、誘導開始5~6日目に活性化し、その後発現が弱くなることが判明した。また、生殖細胞系列や初期胚で機能するPrdm14遺伝子は、mEpiSCでは極めて低い発現しか見られなかったが、iBLCでは発現が誘導されていた。そこで、Prdm14遺伝子の機能をshRNA法で阻害する実験を行ったところ、mEpiSCと誘導5日目までの細胞には目立った影響は観察されなかったが、誘導開始6日目でiBLCの前駆体(iBLC-PC)の細胞が退縮し、iBLCは形成されなかった。これらの結果から、iBLCの誘導にはPrdm14遺伝子の機能が必要であり、その際には2細胞期と同様に、全能性に関わる遺伝子の活性化が生じていることが示された。
続けて、iBLCが本来の胚盤胞の機能をどれだけ再現しているかを検証。胚盤胞を構成する内部細胞塊と栄養外胚葉は、それぞれ異なる遺伝子を発現するが、これらの遺伝子発現を胚盤胞とiBLCで比較したところ、サンプルごとの発現量の差が大きく、発生段階や誘導の程度に幅があることが考えられた。しかし、全体的な傾向として卵割期で発現が誘導される遺伝子群は、胚盤胞と同等の、それ以降で活性化する遺伝子群は胚盤胞より低い発現量だった。一方、胚盤胞の分化に伴い細胞内局在を変えることが知られている転写因子YAPは、iBLCの外側の細胞では核内に局在し、内側の細胞では核外に移行していた。これは、胚盤胞の栄養外胚葉と内部細胞塊で観察される細胞内局在とそれぞれ一致しており、YAPタンパク質はiBLCでも、胚盤胞と同様の核移行制御を受けていることが示唆された。
最後に、iBLCが着床し、個体へと発生する能力を持っているのか、偽妊娠マウスの子宮内移植により確認。その結果、移植による脱落膜の誘導率は、胚盤胞に比べて低いものの、iBLCでのみ観察され、mEpiSCの凝集体や胚様体(EB)では皆無だった。また、この脱落膜を組織観察すると、正常な脱落膜と同様の血管構造や赤血球が見られたことから、母体からの血液が供給されていることがわかった。着床したiBLCは、通常の胚盤胞と同様に増殖および分化の兆しを見せるものの、その後、正常な細胞形態を失って収縮し、胎児吸収と似た状態となって個体へと発生することはなかったという。
再生医療などで利用される多能性幹細胞の質向上を目指す
今回の研究成果は、受精卵などごく限られた細胞にのみ備わる分化全能性や、哺乳類の発生に必須な着床に関わる分子機構の解明に貢献すると期待できる。
研究グループは、「今後、iBLC-PCからiBLCを誘導する培養条件をさらに検討することで、胚盤胞により近いiBLCの誘導を実現し、全能性幹細胞の分化から、着床後の個体発生の再現を目指す。培養条件を改良していくことにより、再生医療などで利用される多能性幹細胞の質を向上させることが可能になるかもしれない」と、述べている。
▼関連リンク
・理化学研究所 プレスリリース




