最低でも1万細胞以上の試料を必要とする従来の「CE-MS分析法」
理化学研究所は7月30日、単一細胞という超微量の生体試料から代謝物を網羅的に計測する超高感度メタボローム分析法を開発したと発表した。この研究は、理研生命機能科学研究センター 一細胞質量分析研究チームの川井隆之研究員、集積バイオデバイス研究チームの太田亘俊研究員、田中陽チームリーダーらの研究チームによるもの。研究成果は、国際科学雑誌「Analytical Chemistry」オンライン版に掲載されている。
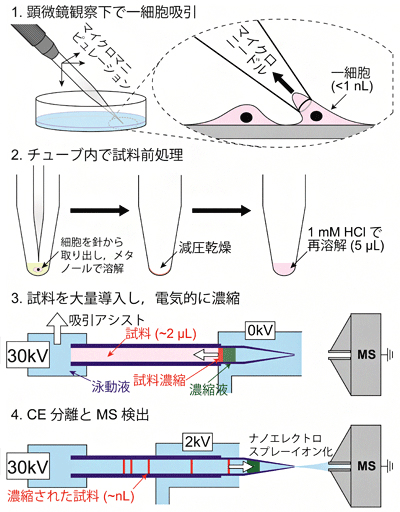
画像はリリースより
特定の細胞や組織、個体での代謝物の種類や濃度を集約した情報(代謝物プロファイル)は、その瞬間の生命活動を直接的に反映していると考えられる。そのため、代謝物を網羅的に解析する「メタボローム分析」により、生命活動の様子を詳細に解析できる。
高性能なメタボローム分析法として、「キャピラリー電気泳動-質量分析(CE-MS)分析法」が知られている。CE-MS分析法は、電気泳動で分離した代謝物を順次エレクトロスプレーイオン化(ESI)法により、イオン化して質量分析法で検出する手法で、定性能と定量性を両立できる優れた分析手法だ。しかし、従来のCE-MS分析法では最低でも1万細胞以上の試料が必要であり、特殊な巨大細胞を除いて、これまで1細胞メタボローム分析は実現していなかった。
nanoCESI法とLDIS法を組み合わせ、従来法の約800倍の超高感度を実現
研究チームは、高性能なCE-MS分析法をさらに大幅に高感度化するため、まず従来のESI法を高効率化した「nanoCESI(Capillary Electrophoresis Sheathless Ionization)法」の開発を行った。開発にあたり、電気泳動での分離に用いる溶融石英製のキャピラリーの先端部分(エミッター)15mm程度をフッ酸やCO2レーザーなどで加工し、壁厚が10マイクロメートル程度で先端径が5~10μmと薄く尖った構造物を作製。これにより、先端から吐出される液滴の初期サイズが小さくなり、さらに先端に電界が収束することから、高効率で安定したエレクトロスプレーを形成できる。このようにして開発したnanoCESIエミッターを用いて、20種類のアミノ酸それぞれの検出感度を調べたところ、従来のESI法と比較して最大で3.5倍の高感度で検出できることがわかった。
次に、nanoCESIエミッターを用いたCE-MS分析により、20種類のアミノ酸混合溶液からそれぞれのアミノ酸の種類と濃度を識別できるかを確認した。分析の結果、全てのアミノ酸を分離し、高感度で検出することに成功。先端が尖っているnanoCESIでは、微小なゴミで閉塞することなく、50回以上の分析を再現よく行うことができた。検出下限の濃度は、リジンの170ピコモーラー、絶対量にして約50万分子に相当する850ゼプトモルと、極めて良好だった。
さらなる高感度化のために、代謝物をキャピラリー内部で濃縮するLDIS法の適用を検討した。LDIS法はキャピラリー内部で試料を2つの異なる原理に基づき、2回濃縮することで、分離性能を損なうことなく高感度化を行う手法で、濃縮のために必要な泳動液はアウトレット側(試料の移動方向側)から引き込む。一方、CE-MSのアウトレット側(キャピラリー先端)は、エレクトロスプレーの形成に特化しており、そのままではLDIS法を適用できない。そこで、泳動液を引き込めるように、キャピラリー先端に液滴を供給することで、LDIS法をCE-MSに適用。これにより、分離性能を損なうことなく、濃縮を適用しないときと比べて最大で380倍もの高感度化に成功した。最終的に、LDIS法とnanoCESI法とを組み合わせることで、従来法と比較して最大で800倍の高感度化を達成し、検出下限の濃度は最高で450フェムトモーラーと、極めて良好だった。この濃度は、東京ドーム40杯分の水に対し、うま味調味料であるグルタミン酸ナトリウム小さじ1杯分に相当するという。
さらに、HeLa細胞1個に含まれる代謝物の網羅解析を行った結果、450種類の代謝物ピークを検出し、そのうち40種類について分子同定を行うことにも成功。この中には、従来の分析法では検出できなかった酸化ストレスマーカーである酸化型グルタチオンなど、さまざまな重要代謝物が含まれており、1細胞ごとの代謝状態が把握できると考えられるという。
今後、nanoCESI法やLDIS法で検出できる代謝物ピークと化合物の対応データベースを拡充していくことにより、より多くの代謝物を同定できるようになると考えられる。さらに、病理切片に含まれる重要な疾患細胞や、血液試料にごく僅かに含まれる疾患細胞などから代謝物プロファイルを取得し、その代謝動態を解明することで、新たな診断法や治療薬の開発につながると期待できる。研究グループは、「今回開発した一連の分析法は、代謝物のみならずタンパク質など他のさまざまな生体関連物質も効率的に濃縮して分析できる手法だ。細胞1個1個のあらゆる生体分子を網羅的に解析することで、新たな生命現象の解明、疾患メカニズムの解明など、医療・創薬に限らずあらゆる生命科学研究への貢献が期待できる」と、述べている。
▼関連リンク
・理化学研究所 プレスリリース



