TRPC6変異がFSGS発症にどう関与するのか
京都大学は7月10日、腎病変の1つである巣状糸球体硬化症(Focal segmental glomerulosclerosis:FSGS)の発症メカニズムを分子および細胞レベルで解明したと発表した。この研究は、同大大学院工学研究科森誠之准教授(研究当時、現:産業医科大学医学部教授)、オノーポラット同博士課程学生、宇野雅俊同博士課程学生、京都大学大学院理学研究科杤尾豪人教授らの研究グループによるもの。研究成果は「Journal of American Society of Nephrology」に掲載されている。
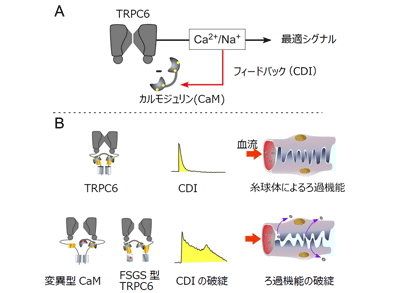
画像はリリースより
近年、高齢者のみならず就労年齢における腎疾患患者数、腎臓透析患者の増加傾向が続いており、腎機能破綻機構の解明と治療戦略の明確化が急務になってきている。FSGSは、腎臓の機能不全を引き起こす可能性のある代表的な腎病変の1つで、多くがステロイド治療に抵抗性を示す。15年ほど前、家族性FSGSの遺伝学的解析から、カルシウムチャネルの1つTRPC6チャネルの変異がこの病変に関連していることが報告され、以来、30種類近くのTRPC6変異体が世界中のさまざまな地域に住む患者から見つかっている。しかし変異が生じると何が起きて、何が問題になるのか、詳細は不明のままであり原因究明が求められていた。
CDIの破綻がFSGSの発症原因に
TRPC6はCa2+(カルシウムイオン)を細胞内に透過する膜タンパク質の1つで、細胞内Ca2+依存的に不活性化する、Ca2+-dependent inactivation(CDI)と呼ばれる自己抑制的(ブレーキ)機構を保持している。研究グループはこのCDI機構がどのようにして起こるのかを明らかにするため、細胞内カルシウム結合タンパク質「カルモジュリン(CaM)」やTRPC6のcoiled-coil ドメインを介した分子複合体構造について、NMR(核磁気共鳴法)やFRET(蛍光共鳴エネルギー移動)等の手法を用いて解析した。その結果、Ca2+と結合したCaMがTRPC6のcoiled-coilドメイン近傍において橋渡し的に相互作用することでCDIを生じさせているメカニズムを発見。TRPC6のcoiled-coilドメインにはFSGSの変異が多数報告されていたことから、変異型coiled-coilドメインの複合体形成に関して解析したところ、FSGS型coiled-coilドメインは標準型に比べ複合体形成において強弱が見られた。また電気生理学的に機能的な解析をしたところ、評価した5種類全てのFSGS型TRPC6において顕著なCDIの遅延を認めた。さらにFSGS型TRPC6チャネルやCDI遅延を引き起こすCaMの変異体をポドサイトに発現させたところ、細胞骨格(アクチンフィラメント)において病態様構造変化が引き起こされることを確認した。これはCDIの破綻がFSGSの原因になることを初めて分子、細胞レベルで示唆する結果だ。
今回の研究結果はTRPC6チャネルの不活性化機構の発端を明らかにする基礎研究であると共に、CDIの破綻がFSGSの発症原因であるという新しい概念を提唱するもの。「日本人にもTRPC6原因でFSGSを発症する患者が報告されているが、今回の研究はFSGSの治療に際しTRPC6チャネル活性を抑制することが重要であることを分子的に証明するものでもあり、今後の治療へ向け大きな足がかりになる」と、研究グループは述べている。
▼関連リンク
・京都大学 研究成果



